
| 选项 | 实验目的 | 实验方案 |
| A | 检验Fe2O3中是否含有FeO | 向少量固体样品中加入适量稀硝酸溶解后,再滴加少量的高锰酸钾溶解 |
| B | 测定NaHCO3和NH4Cl固体混合物中NaHCO3 的质量分数 | 准确称取ag样品和坩埚总质量,加强热后在空 气中冷却至室温,再称量得到总质量为bg |
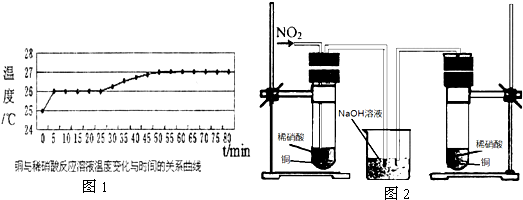
| C | 探究温度对化学平衡的影响 | 把装有颜色相同的NO2和N2O4混合气体的两支试管(密封)分别浸入冷水和热水中 |
| D | 除去CO2气体中混有的少量HCl气体 | 将混合气体依次通过盛有饱和Na2CO3溶液和浓H2SO4的洗气瓶 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.稀硝酸具有强氧化性,能够将氧化铁离子氧化成铁离子;
B.碳酸钠易吸水变质,不能直接在空气中冷却加热后固体;
C.根据混合气体在冷水、热水中颜色深浅可判断温度对可逆反应的影响;
D.二氧化碳与碳酸钠反应,应该用饱和碳酸氢钠溶液.
解答 解:A.检验Fe2O3中是否含有FeO,先用酸溶解固体,可用稀硫酸,不能用强氧化性的稀硝酸,否则亚铁离子被氧化成铁离子,干扰了检验结果,故A错误;
B.测定NaHCO3和NH4Cl固体混合物中NaHCO3的质量分数,准确称取ag样品和坩埚总质量,加强热后在干燥器冷却至室温,再称量得到总质量为bg,不能直接在空气中冷却,否则影响测定结果,故B错误;
C.把装有颜色相同的NO2和N2O4混合气体的两支试管(密封)分别浸入冷水和热水中,根据混合气体颜色变化可判断温度对反应速率的影响,故C正确;
D.除去CO2气体中混有的少量HCl气体,将混合气体依次通过盛有饱和NaHCO3溶液和浓H2SO4的洗气瓶,由于二氧化碳与碳酸钠反应,所以不能用碳酸钠溶液,故D错误;
故选C.
点评 本题考查了化学实验方案的设计与评价,题目难度中等,明确常见元素化合物性质为解答关键,注意熟练掌握化学实验基本操作方法,试题培养了学生的分析能力及灵活应用能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 成语、谚语、俗语 | 理解或寓意 |
| A | “甘之如饴” | 糖类均有甜味 |
| B | “冰、水为之,而寒于水” | 相同质量和温度的水和冰,冰的能量高 |
| C | “雷雨肥庄稼” | 农作物生长需要水,雷雨天提供了大量的雨水 |
| D | “春蚕到死丝方尽” | 蚕丝的只要成分是蛋白质 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸氢钠 | B. | 氢氧化铝 | C. | 碳酸镁 | D. | 硫酸钡 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,则其在周期表中的位置是第四周期,第ⅤA族.
,则其在周期表中的位置是第四周期,第ⅤA族.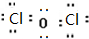 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O在高温下难分解,H2S在300℃即分解,说明氧的非金属性比硫强 | |
| B. | I-的还原性比Br-强,由此可推断溴的非金属性比碘强 | |
| C. | H2CO3的酸性比HClO的酸性强,说明碳的非金属性比氯强 | |
| D. | 已知反应:2NH3+3Cl2═N2+6HCl,由此可推断非金属性氯强于氮 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com