
 CO2��g����H2��g�����仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
CO2��g����H2��g�����仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���| t�� | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.5 |
| A��������ѹǿ���� | B�����������c��CO������ |
| C���ԣ�����H2�����ԣ��棬H2O�� | D��c��CO2����c��CO�� |
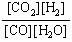 �������ȣ���BC����830��
�������ȣ���BC����830��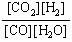 ���ƻ�ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ��֪�������¶����ߣ�ƽ�ⳣ������������ӦΪ���ȷ�Ӧ���Ƿ�Ӧ����ʽǰ��ϵ����ȣ�ѹǿʼ�ղ��䣬�����ж�ƽ���Ƿ��ƽ��״̬����B˵����������C˵�����ȡ������߾����ж��Ѵ�ƽ��״̬��Dֻ��Ũ����ȣ�������Ũ�ȱ��ֲ��䣬���������жϷ�Ӧ�Ѵ�ƽ��״̬����c��CO2����c��H2����c��CO����c��H2O����˵��ƽ�ⳣ��KΪ1������Ӧ���¶���830�档
���ƻ�ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ��֪�������¶����ߣ�ƽ�ⳣ������������ӦΪ���ȷ�Ӧ���Ƿ�Ӧ����ʽǰ��ϵ����ȣ�ѹǿʼ�ղ��䣬�����ж�ƽ���Ƿ��ƽ��״̬����B˵����������C˵�����ȡ������߾����ж��Ѵ�ƽ��״̬��Dֻ��Ũ����ȣ�������Ũ�ȱ��ֲ��䣬���������жϷ�Ӧ�Ѵ�ƽ��״̬����c��CO2����c��H2����c��CO����c��H2O����˵��ƽ�ⳣ��KΪ1������Ӧ���¶���830�档


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2Z��ӦӰ���ʾ��ͼ��ͼ�к������ʾ�¶ȣ��������ʾƽ����������Z���������������������ȷ����(����)
2Z��ӦӰ���ʾ��ͼ��ͼ�к������ʾ�¶ȣ��������ʾƽ����������Z���������������������ȷ����(����)
| A���������淴Ӧ������ӦΪ���ȷ�Ӧ |
| B��X��Y��Z������ |
| C��X��Y��ֻ��һ��Ϊ��̬��ZΪ��̬ |
| D��������Ӧ���淴Ӧ��H��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 CO2��g��+H2��g����һ��ʱ���÷�Ӧ�ﵽƽ�⣬���CO�����ʵ���Ϊ0.5 mol��������˵����ȷ����
CO2��g��+H2��g����һ��ʱ���÷�Ӧ�ﵽƽ�⣬���CO�����ʵ���Ϊ0.5 mol��������˵����ȷ����| A��800���£��÷�Ӧ�Ļ�ѧƽ�ⳣ��Ϊ0.25 |
| B��427��ʱ�÷�Ӧ��ƽ�ⳣ��Ϊ9.4����÷�Ӧ�ġ�H��0 |
| C��ͬ���£����������ƽ����ϵ��ͨ��1.0 mol��H2O��g������ƽ��ʱCOת����Ϊ66.7% |
| D��ͬ���£����������ƽ����ϵ��ͨ��1.0 mol��CO��g������ƽ��ʱCO���ʵ�������Ϊ33.3% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
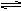 CO2(g)��H2(g)����Ӧ�ﵽƽ��ʱ�����CO��ת����Ϊ21.75%����ƽ��ʱ��������ܶ�Ϊ��ͬ������H2�ܶȵģ� ��
CO2(g)��H2(g)����Ӧ�ﵽƽ��ʱ�����CO��ת����Ϊ21.75%����ƽ��ʱ��������ܶ�Ϊ��ͬ������H2�ܶȵģ� ��| A��11.5�� | B��15.75�� | C��23�� | D��46�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��SO2��ת����Ϊ60% |
| B��SO3�IJ���Ϊ50% |
| C��ƽ��ʱ��ѹǿ����ʼѹǿ֮��Ϊ7��8 |
| D��ƽ��ʱVSO2��VO2��VSO3��3��3��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
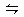 2NO��g����O2��g������ʱ��Ӧ�ﵽƽ��״̬�ı�־�ǣ� ��
2NO��g����O2��g������ʱ��Ӧ�ﵽƽ��״̬�ı�־�ǣ� ��| A�����������ܶȲ��ٱ仯 |
| B������������ɫ��dz |
| C�����������NO2��NO��O2�����ʵ���֮��Ϊ2��2��1 |
| D����λʱ��������2n mol NO��ͬʱ����2n mol NO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
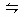 2Z��g����H��0��Ϊ��ʹƽ��������Z�ķ����ƶ���Ӧ��ȡ�Ĵ�ʩ�ǣ� ��
2Z��g����H��0��Ϊ��ʹƽ��������Z�ķ����ƶ���Ӧ��ȡ�Ĵ�ʩ�ǣ� ��| A���٢ۢ� | B���ڢۢ� | C���ڢۢ� | D���ڢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
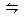 p C(g)���ﵽƽ��������������ѹ����ԭ����һ�룬���ٴ�ƽ��ʱC����Һ��ԭ����1.9����������������ȷ���� ( )
p C(g)���ﵽƽ��������������ѹ����ԭ����һ�룬���ٴ�ƽ��ʱC����Һ��ԭ����1.9����������������ȷ���� ( )| A��ƽ��������Ӧ�����ƶ� | B��C����������������� |
| C������A��ת���ʽ��� | D��m��n��p |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com