
| 起始浓度 | 甲 | 乙 | 丙 |
| c(N2)/mol•L-1 | 0.46 | 0.46 | 0.92 |
| c(O2)/mol•L-1 | 0.46 | 0.23 | 0.92 |
| A. | 起始时,反应速率:丙>甲>乙 | B. | 平衡时,c(NO):甲=丙>乙 | ||
| C. | 平衡时,N2的转化率:甲>乙 | D. | 平衡时,甲中c(N2)=0.4 mol•L-1 |
分析 A.反应物初始浓度越大,容器内压强越大,则反应起始速率越快;
B.该反应为气体体积不变的反应,平衡时丙中NO浓度为甲的2倍,即c(NO):2甲=丙;
C.甲与乙相比,甲相当于在乙的基础上增大氧气的浓度,则甲中氮气的转化率较大;
D.设平衡时氮气消耗浓度为x,然后利用平衡常数表达式列式计算.
解答 解:A.在t℃下甲、乙、丙三个恒容密闭容器中,反应初始总浓度越大反应速率越快,起始时总浓度大小为:丙>甲>乙,则起始时反应速率:丙>甲>乙,故A正确;
B.反应N2(g)+O2(g)?2NO(g)为气体体积不变的反应,压强不影响化学平衡,则平衡时平衡时丙中NO浓度为甲的2倍,即c(NO):2甲=丙、甲>乙,故B错误;
C.甲、乙中氮气的浓度相等,甲相当于在乙的基础上增大氧气的浓度,则甲中氮气的转化率较大,即平衡时N2的转化率:甲>乙,故C正确;
D.t℃时,K=0.09,设甲容器平衡时氮气消耗的浓度为x,
N2(g)+O2(g)?2NO(g)
初始(mol/L)0.46 0.46 0
转化(mol/L)x x 2x
平衡(mol/L)0.46-x 0.46-x 2x
则平衡常数K=$\frac{({2x)}^{2}}{(0.46-x)(0.46-x)}$=0.09,解得x=0.06mol/L,所以平衡时甲中c(N2)=0.4 mol•L-1,故D正确;
故选B.
点评 本题考查化学平衡的计算,题目难度中等,涉及化学平衡、化学反应速率的影响、化学平衡的计算等知识,明确化学平衡及其影响为解答关键,注意掌握三段式在化学平衡计算中的应用.


 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案科目:高中化学 来源: 题型:实验题
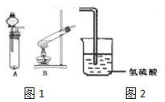 某研究性学习小组设计了一组实验来验证元素周期律.
某研究性学习小组设计了一组实验来验证元素周期律.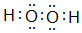 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:推断题
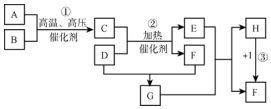
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
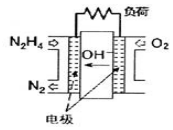 肼(N2H4)-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.下列说法中,不正确的是( )
肼(N2H4)-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.下列说法中,不正确的是( )| A. | 该电池放电时,通入肼的一极为负极 | |
| B. | 电池每释放1mol N2转移的电子数为4NA | |
| C. | 通入空气的一极的电极反应式是:O2+4e-+4H+=2H2O | |
| D. | 电池工作一段时间后,电解质溶液的pH将减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图X为电源,椭圆形滤纸Y浸透饱和食盐水和酚酞试液,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向c端扩散.下列判断正确的是( )
如图X为电源,椭圆形滤纸Y浸透饱和食盐水和酚酞试液,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向c端扩散.下列判断正确的是( )| A. | b为电源的正极,d点周围变红 | B. | Cu电极质量减小,Pt电极质量增大 | ||
| C. | Z中溶液的pH先减小,后增大 | D. | 溶液中的SO42-向Pt电极定向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
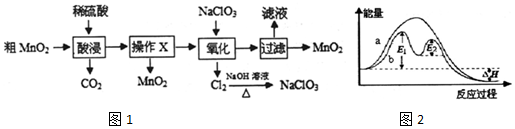
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
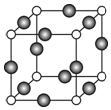 已知X、Y、Z、W、K五种元素均位于周期表的前四周期,且原子序数依次增大.元素X是周期表中原子半径最小的元素;Y的基态原子中电子占据了三种能量不同的原子轨道,且这三种轨道中的电子数相同;W位于第2周期,其原子的核外成对电子数是未成对电子数的3倍;K位于ds区且原子的最外层电子数与X的相同.
已知X、Y、Z、W、K五种元素均位于周期表的前四周期,且原子序数依次增大.元素X是周期表中原子半径最小的元素;Y的基态原子中电子占据了三种能量不同的原子轨道,且这三种轨道中的电子数相同;W位于第2周期,其原子的核外成对电子数是未成对电子数的3倍;K位于ds区且原子的最外层电子数与X的相同.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com