
【题目】按题目要求答题:
(1)(CH3)2CHCH(CH3)CH2CH3的系统命名是
(2)写出苯与液溴发生取代反应的化学方程式:
(3)某烃A的相对分子质量为84,能与氢气发生加成反应.A的一氯取代产物只有一种,则A的结构简式为 .
【答案】
(1)2,3﹣二甲基戊烷
(2)C6H6+Br2 ![]() C6H5Br+HBr
C6H5Br+HBr
(3)![]()
【解析】解:(1)烷烃命名时,要选最长的碳链为主链,故主链上有5个碳原子,故为戊烷,从离支链近的一端给主链上碳原子编号,故在2号和3号碳原子上各有一个甲基,故名称为2,3﹣二甲基戊烷, 所以答案是:2,3﹣二甲基戊烷;(2)苯与溴发生取代反应生成溴苯和HCl,该反应为C6H6+Br2 ![]() C6H5Br+HBr,
C6H5Br+HBr,
所以答案是:C6H6+Br2 ![]() C6H5Br+HBr;(3)含有1个碳碳双键,则A应为烯烃,设分子式为CnH2n , 相对分子质量为84,则有14n=84,n=6,A的一氯取代产物只有一种说明分子中只有一种类型的氢,说明结构对称,即双键C上的4个H均被甲基取代,其结构简式应为
C6H5Br+HBr;(3)含有1个碳碳双键,则A应为烯烃,设分子式为CnH2n , 相对分子质量为84,则有14n=84,n=6,A的一氯取代产物只有一种说明分子中只有一种类型的氢,说明结构对称,即双键C上的4个H均被甲基取代,其结构简式应为 ![]() ,
,
所以答案是: ![]() .
.


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
【题目】在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如右图所示,由此确定,原溶液中含有的阳离子是:

A. Mg2+、Al3+、Fe2+ B. H+、Mg2+、Al3+
C. H+、Ba2+、Al3+ D. 只有Mg2+、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在生产生活中,我们会遇到各种各样的化学反应。请按要求回答下列问题:
(1)焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质:NH4Cl、N2、Fe2O3、Fe、FeCl3 和 X。
①根据题意,可判断出X是_____________(写化学式)
②写出并配平该反应的化学方程式,并用双线桥标出电子转移的方向和数目:______。
(2)铝元素是自然界中含量最多的的金属元素,应用广泛。金属铝既能与酸反应又能与强碱反应,请写出铝与强碱反应的离子方程式__________________________________________ 。
(3)Na2O2可用作呼吸面具的供氧剂, 发生反应的化学方程式为__________________________。
(4)“水玻璃”长期暴露在空气中会变质,这是因为“水玻璃”与空气中少量二氧化碳接触,生成了乳白色的凝胶状沉淀的缘故。写出反应的离子方程式_________________________________。
(5)小苏打可作胃药,请写出其中和胃酸时的离子方程式______________________ 。
(6)在反应 3BrF3+5H2O = HBrO3+Br2+9HF+O2 中,被氧化的元素是____________,当有5 mol水反应时,由H2O还原的BrF3为______________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境污染已成为人类社会面临的重大问题,各种污染数不胜数。导致下列污染的主要原因与高分子化合物有关的是( )
A. 酸雨 B. 光化学烟雾
C. 温室效应 D. 白色污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.合成纤维和人造纤维统称为化学纤维
B.聚氯乙烯是热固性塑料
C.锦纶丝接近火焰时先蜷缩,燃烧时有烧焦羽毛的气味,灰烬为有光泽的硬块,能压成粉末
D.对于某些合成材料和塑料制品废弃物的处理可以倾倒到海洋中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,属于氧化还原反应的是( )
A. CaO+H2O=Ca(OH)2 B. CaCO3![]() CaO+CO2↑
CaO+CO2↑
C. CH4+2O2![]() 2H2O+CO2↑ D. Na2CO3+2HCl=2NaCl+H2O+CO2↑
2H2O+CO2↑ D. Na2CO3+2HCl=2NaCl+H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不另用任何试剂就能将下列四种溶液:①CuSO4、②Na2SO4、③KCl、④BaCl2鉴别出来,其正确的鉴别顺序是 ( )
A.①②④③B.④③②①C.①④②③D.②①④③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某些电镀厂的酸性废水中常含有一定量的CrO42﹣和Cr2O72﹣ , 它们会对人类及生态系统产生很大的伤害,必须进行处理.常用的处理方法有两种
方法1:还原沉淀法,其中第①步存在平衡步存在平衡:2CrO42﹣(黄色)+2H+Cr2O72﹣(橙色)+H2O
(1)若平衡体系的pH=12,该溶液显 .
(2)写出第③步的离子反应方程式: .
(3)第②步中,用6mol的FeSO47H2O可还原molCr2O72﹣离子.
(4)第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3() Cr3+(aq)+3OH﹣(aq)
常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)c3(OH﹣)=10﹣32 , 要使c(Cr3+)降至10﹣5mol/L,溶液的pH应调至 .
方法2:电解法:该法用Fe做电极电解含Cr2O72﹣的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀.
(5)写出阳极的电极反应式 .
(6)在阴极附近溶液pH升高的原因是(用电极反应解释)
(7)用电镀法在铁制品上镀上一层锌,则阴极上的电极反应式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按下列要求填空:
(1)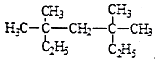 系统命名法为;
系统命名法为;
(2)键线式 ![]() 表示的有机物的结构简式是;
表示的有机物的结构简式是;
(3)醇分子中各化学键如图所示,对乙醇在各种反应中应断裂的键说明正确的是 
①和金属钠作用时,断裂;
②和浓硫酸共热至170℃时,断裂;
③和乙酸、浓硫酸共热时,断裂;
④在铜催化下和氧气反应时,断裂;
⑤与氢卤酸反应时,断裂;
(4)分子质量为70的烯烃的分子式为 , 若该烯烃与足量H2加成后能生成含3个甲基的烷烃,则该烯烃可能的结构简式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com