
| A£® | »·±£ČČ“Ź”°PM2.5”±ŹĒÖø“óĘųÖŠÖ±¾¶Š”ÓŚ»ņµČÓŚ2.5 Ī¢Ć×£Ø1Ī¢Ć×=1”Į10-6Ć×£©µÄæÅĮ££¬”°PM2.5”±ÓėæÕĘųŠĪ³ÉµÄ·ÖÉ¢ĻµŹōÓŚ½ŗĢå | |
| B£® | Ź³ŃĪÖŠ¼ÓČėÉŁĮæµā»Æ¼Ų£¬Ź³ÓĆŗóæɲ¹³äČĖĢåÄŚµāŌŖĖŲµÄ²»×ć | |
| C£® | ŹÆÓĶ“ß»ÆĮŃ»ÆµÄÖ÷ŅŖÄæµÄŹĒĢįøßĘūÓĶµČĒįÖŹÓĶµÄ²śĮæÓėÖŹĮ棬ŹÆÓĶĮŃ½āµÄÖ÷ŅŖÄæµÄŹĒµĆµ½øü¶ąµÄŅŅĻ©”¢±ūĻ©µČĘųĢ¬¶ĢĮ“Ģž | |
| D£® | ¾§Ģå¹čŹĒĶ؊Ź¤³ĢÖŠÖĘ×÷¹āµ¼ĻĖĪ¬µÄÖ÷ŅŖŌĮĻ |
·ÖĪö A£®·ÖÉ¢ÖŹĮ£×ÓÖ±¾¶ŌŚ1nm”«100nmÖ®¼äµÄ·ÖÉ¢ĻµŹōÓŚ½ŗĢ壻
B£®ŃĪÖŠĢķ¼ÓÉŁĮæµāĖį¼Ų£»
C£®ŹÆÓĶĮŃ»ÆŹĒ½«ÖŲÓĶ×Ŗ»ÆĪŖĒįÖŹÓĶ£¬ĮŃ½āŹĒµĆµ½Š”·Ö×ÓµÄĻ©ĢžµČ£»
D£®¾§Ģå¹čƻӊµ¼¹āŠŌ£¬²»ÄÜÖĘ×÷¹āµ¼ĻĖĪ¬£®
½ā“š ½ā£ŗA£®PM2.5·ÖÉ¢ŌŚæÕĘųÖŠæÉÄÜŠĪ³É½ŗĢ壬¹ŹA“ķĪó£»
B£®ŃĪÖŠĢķ¼ÓÉŁĮæµāĖį¼Ų£¬²»ŹĒµā»Æ¼Ų£¬¹ŹB“ķĪó£»
C£®ŹÆÓĶ“ß»ÆĮŃ»ÆµÄÄæµÄŹĒĢįøßĘūÓĶµČĒįÖŹÓĶµÄ²śĮæÓėÖŹĮ棬ĮŃ½āµÄÄæµÄŹĒµĆµ½Š”·Ö×ÓµÄĻ©Ģž£¬¹ŹCÕżČ·£»
D£®¾§Ģå¹čƻӊµ¼¹āŠŌ£¬²»ÄÜÖĘ×÷¹āµ¼ĻĖĪ¬£¬ÖĘ×÷¹āµ¼ĻĖĪ¬µÄ²ÄĮĻŹĒ¶žŃõ»Æ¹č¾§Ģ壬¹ŹD“ķĪó£®
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²é»ÆѧÓėÉś»ī£¬Ć÷Č·ŌŖĖŲµÄµ„ÖŹ¼°Ęä»ÆŗĻĪļµÄŠŌÖŹŹĒ½ā¾ö±¾ĢāµÄ¹Ų¼ü£¬ĢāÄæÄŃ¶Č²»“ó£®


 100·Ö“³¹ŲĘŚÄ©³å“ĢĻµĮŠ“š°ø
100·Ö“³¹ŲĘŚÄ©³å“ĢĻµĮŠ“š°ø ĆūŠ£ĮŖĆĖæģĄÖæĪĢĆĻµĮŠ“š°ø
ĆūŠ£ĮŖĆĖæģĄÖæĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | õ„ĄąĪļÖŹŹĒŠĪ³ÉĖ®¹ūĻćĪ¶µÄÖ÷ŅŖ³É·Ö | |
| B£® | ÓĶÖ¬µÄŌķ»Æ·“Ӧɜ³ÉÖ¬·¾ĖįŗĶ±ū“¼ | |
| C£® | µ°°×ÖŹµÄĖ®½ā²śĪļ¶¼ŗ¬ÓŠČ©»łŗĶ°±»ł | |
| D£® | ĢĒĄą»ÆŗĻĪļ¶¼¾ßÓŠĻąĶ¬µÄ¹ŁÄÜĶÅ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
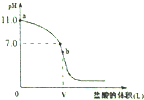 ³£ĪĀŹ±£¬ĻņÅضČĪŖ0.1mol/LĢå»żĪŖV LµÄ°±Ė®ÖŠÖšµĪ¼ÓČėŅ»¶ØÅØ¶ČµÄŃĪĖį£¬ÓĆpH¼Ę²āµĆČÜŅŗµÄpHĖęŃĪĖįµÄ¼ÓČėĮæ¶ų±ä»ÆµÄµĪ¶ØĒśĻßČēĶ¼ĖłŹ¾£¬bµć±ķŹ¾Į½ÖÖČÜŅŗĒ”ŗĆĶźČ«·“Ó¦£®
³£ĪĀŹ±£¬ĻņÅضČĪŖ0.1mol/LĢå»żĪŖV LµÄ°±Ė®ÖŠÖšµĪ¼ÓČėŅ»¶ØÅØ¶ČµÄŃĪĖį£¬ÓĆpH¼Ę²āµĆČÜŅŗµÄpHĖęŃĪĖįµÄ¼ÓČėĮæ¶ų±ä»ÆµÄµĪ¶ØĒśĻßČēĶ¼ĖłŹ¾£¬bµć±ķŹ¾Į½ÖÖČÜŅŗĒ”ŗĆĶźČ«·“Ó¦£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

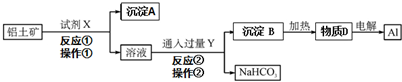
| A£® | ¼×µē¼«ĪŖŅõ¼« | |
| B£® | ĪŖŹ¹µē½ā²śĪļČ«²æ×Ŗ»ÆĪŖNH4NO3£¬Šč²¹³äµÄĪļÖŹĪŖNH3 | |
| C£® | ŅŅµē¼«µÄµē¼«·“Ó¦Ź½ŹĒ£ŗNO-3e-+4OH-=NO3-+2H2O | |
| D£® | øĆ·“Ó¦ÖŠNO¼ČŹĒŃõ»Æ¼ĮÓÖŹĒ»¹Ō¼Į |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2H2£Øg£©+O2£Øg£©=2H2O£Øg£©”÷H1£» 2H2£Øg£©+O2£Øg£©=2H2O£Øl£©”÷H2 | |
| B£® | S£Øg£©+O2£Øg£©=SO2£Øg£©”÷H1£» S£Øs£©+O2£Øg£©=SO2£Øg£©”÷H2 | |
| C£® | $\frac{1}{2}$C£Øs£©+O2£Øg£©=CO£Øg£©”÷H1£» C£Øs£©+O2£Øg£©=CO2£Øg£©”÷H2 | |
| D£® | HCl£Øg£©=$\frac{1}{2}$H2£Øg£©+$\frac{1}{2}$Cl2£Øg£©”÷H1£» H2£Øg£©+Cl2£Øg£©=2HCl£Øg£©”÷H2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  ³żČ„COµÄCO2 | B£® |  ŻĶČ”Ź±Õńµ“»ģŗĻŅŗ | ||
| C£® | 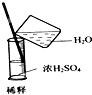 Ļ”ŹĶÅØĮņĖį | D£® |  ĻņŹŌ¹ÜÖŠµĪ¼ÓŅŗĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com