£Ø2011?±¦¼¦Ņ»Ä££©¢ń£®µŖŹĒµŲĒņÉĻŗ¬Įæ×ī·įø»µÄŅ»ÖÖŌŖĖŲ£¬µŖ¼°Ęä»ÆŗĻĪļŌŚ¹¤Å©ŅµÉś²ś”¢Éś»īÖŠÓŠ×ÅÖŲŅŖ×÷ÓĆ£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
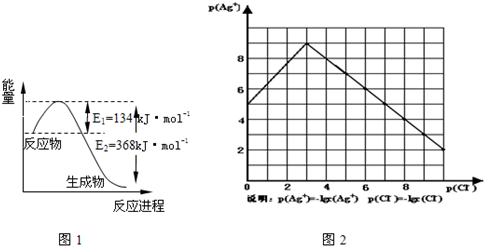
£Ø1£©Ķ¼1ŹĒ1mol NO
2ŗĶ1mol CO·“Ӧɜ³ÉCO
2ŗĶNO¹ż³ĢÖŠÄÜĮæ±ä»ÆŹ¾ŅāĶ¼£¬ĒėŠ“³öNO
2ŗĶ CO·“Ó¦µÄČČ»Æѧ·½³ĢŹ½
NO2£Øg£©+CO£Øg£©ØTCO2£Øg£©+NO£Øg£©”÷H=-234kJ?mol-1
NO2£Øg£©+CO£Øg£©ØTCO2£Øg£©+NO£Øg£©”÷H=-234kJ?mol-1
| t/”ę |
200 |
300 |
400 |
| K |
K1 |
K2 |
0.5 |
£Ø2£©ŌŚ0.5LµÄĆܱÕČŻĘ÷ÖŠ£¬Ņ»¶ØĮæµÄµŖĘųŗĶĒāĘų½ųŠŠČēĻĀ»Æѧ·“Ó¦£ŗN
2£Øg£©+3H
2£Øg£©?2NH
3£Øg£©”÷H£¼0£¬Ęä»ÆŃ§Ę½ŗā³£ŹżKÓėĪĀ¶ČtµÄ¹ŲĻµČē±ķ£ŗĒėĶź³ÉĻĀĮŠĪŹĢā£»
¢ŁŹŌ±Č½ĻK
1ӢK
2µÄ“󊔣¬K
1£¾
£¾
K
2£ØĢīŠ“”°£¾”±”¢”°=”±»ņ”°£¼”±£©
¢ŚĻĀĮŠø÷ĻīÄÜ×÷ĪŖÅŠ¶ĻøĆ·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄŅĄ¾ŻŹĒ
c
c
£ØĢīŠņŗÅ×ÖÄø£©
a£®ČŻĘ÷ÄŚN
2ӢH
2ӢNH
3µÄÅضČÖ®±ČĪŖ1£ŗ3£ŗ2 b£®¦Ō£ØN
2£©£ØÕż£©=3¦Ō£ØH
2£©£ØÄę£©
c£®ČŻĘ÷ÄŚŃ¹Ēæ±£³Ö²»±ä d£®»ģŗĻĘųĢåµÄĆܶȱ£³Ö²»±ä
¢Ū400”ꏱ£¬·“Ó¦2NH
3£Øg£©?N
2£Øg£©+3H
2£Øg£©µÄ»ÆŃ§Ę½ŗā³£ŹżµÄÖµĪŖ
2
2
£®µ±²āµĆNH
3ŗĶN
2ӢH
2µÄĪļÖŹµÄĮæ·Ö±šĪŖ3molŗĶ2mol”¢1molŹ±£¬ŌņøĆ·“Ó¦µÄ
¦Ō£ØN
2£©£ØÕż£©
£¾
£¾
¦Ō£ØN
2£©£ØÄę£© £ØĢīŠ“”°£¾”±”¢”°=”±»ņ”°£¼”±=£©
¢ņ£®³ĮµķĪļ²¢·Ē¾ų¶Ō²»ČÜ£¬ĒŅŌŚĖ®¼°ø÷ÖÖ²»Ķ¬µÄČÜŅŗÖŠČܽā¶ČÓŠĖł²»Ķ¬£¬Ķ¬Ąė×ÓŠ§Ó¦”¢ĀēŗĻ
ĪļµÄŠĪ³ÉµČ¶¼»įŹ¹³ĮµķĪļµÄČܽā¶ČÓŠĖłøı䣮ŅŃÖŖAgCl+Cl
-ØT[AgCl
2]
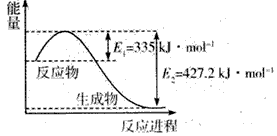
-£¬Ķ¼2ŹĒijĪĀ¶ČĻĀAgClŌŚNaClČÜŅŗÖŠµÄČܽāĒéæö£®
ÓÉŅŌÉĻŠÅĻ¢æÉÖŖ£ŗ
£Ø1£©ÓÉĶ¼ÖŖøĆĪĀ¶ČĻĀAgClµÄČܶȻż³£ŹżĪŖ
10-12
10-12
£®
£Ø2£©AgClŌŚNaClČÜŅŗÖŠµÄČܽā³öĻÖČēĶ¼ĖłŹ¾Ēéæö£ØĻȱ䊔ŗó±ä“󣩵ÄŌŅņŹĒ£ŗ
Cl-ŅÖÖĘĮĖAgClµÄČܽā£¬µ«Cl-ÅضČŌö“óŹ¹AgClŠĪ³ÉĀēŗĻĪļ£ŗAgCl+Cl-ØT[AgCl2]-
Cl-ŅÖÖĘĮĖAgClµÄČܽā£¬µ«Cl-ÅضČŌö“óŹ¹AgClŠĪ³ÉĀēŗĻĪļ£ŗAgCl+Cl-ØT[AgCl2]-
£Ø3£©Éč¼ĘŹµŃéÖ¤Ć÷S£ØAgCl£©£¾S£ØAgI£©£¾S£ØAg
2S£©£¬ŹµŃé·½°øŹĒ
ĻņAgClŠü×ĒŅŗÖŠµĪ¼ÓKIĻ”ČÜŅŗ£Ø0.1mol/L£©£¬¹ĢĢåÓÉ°×É«×Ŗ»ÆĪŖ»ĘÉ«£¬ŌŁĻņŠü×ĒŅŗÖŠµĪ¼ÓĶ¬ÅضČNa2SĻ”ČÜŅŗ£Ø0.1mol/L£©£¬¹ĢĢåÓÉ»ĘÉ«×Ŗ»ÆĪŖŗŚÉ«
ĻņAgClŠü×ĒŅŗÖŠµĪ¼ÓKIĻ”ČÜŅŗ£Ø0.1mol/L£©£¬¹ĢĢåÓÉ°×É«×Ŗ»ÆĪŖ»ĘÉ«£¬ŌŁĻņŠü×ĒŅŗÖŠµĪ¼ÓĶ¬ÅضČNa2SĻ”ČÜŅŗ£Ø0.1mol/L£©£¬¹ĢĢåÓÉ»ĘÉ«×Ŗ»ÆĪŖŗŚÉ«
£®
£Ø4£©ČōŌŚAgClŠĪ³ÉµÄ×ĒŅŗÖŠµĪ¼Ó°±Ė®ÓŠŹ²Ć“ĻÖĻó£æ
°×É«³ĮµķČܽā£¬ŠĪ³ÉĪŽÉ«ČÜŅŗ
°×É«³ĮµķČܽā£¬ŠĪ³ÉĪŽÉ«ČÜŅŗ
£®·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ
AgCl+2NH3=Ag£ØNH3£©2++Cl-
AgCl+2NH3=Ag£ØNH3£©2++Cl-
£®

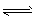 2NH3(g) ”÷H <0£¬ÓŠČēĻĀŹż¾Ż£ŗ
2NH3(g) ”÷H <0£¬ÓŠČēĻĀŹż¾Ż£ŗ 
 ½Ģ²ÄČ«½ā×Ö“Ź¾äĘŖĻµĮŠ“š°ø
½Ģ²ÄČ«½ā×Ö“Ź¾äĘŖĻµĮŠ“š°ø


