
分析 MnO2中Mn4+核外电子排布式为1s22s22p63s23p63d3,Fe3O4中含有2个Fe3+和一个Fe2+,核外电子排布式分别为:1s22s22p63s23p63d5和1s22s22p63s23p63d6,Cr2O3中,Cr3+核外电子排布式为1s22s22p63s23p63d3,根据电子排布式确定成对电子数,以此解答该题.
解答 解:MnO2中Mn4+核外电子排布式为1s22s22p63s23p63d3,即含有3个未成对电子;Fe3O4中含有2个Fe3+和一个Fe2+,核外电子排布式分别为:1s22s22p63s23p63d5和1s22s22p63s23p63d6,含有5×2+4=14个未成对电子;Cr2O3中,Cr3+核外电子排布式为1s22s22p63s23p63d3,含有2×3个未成对电子,故Fe3O4所含未成对电子最多,磁性最大的是:Fe3O4,
故答案为:Fe3O4.
点评 本题考查电子排布式,为高频考点,侧重于学生的分析能力的考查,注意把握题给信息以及常见元素的核外电子排布,难度不大.


科目:高中化学 来源: 题型:解答题
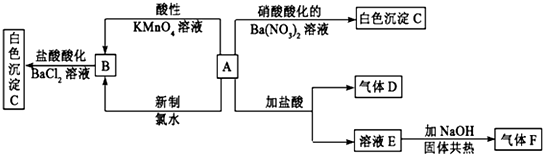
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | CuO作还原剂 | B. | CuO作氧化剂 | ||
| C. | 铜元素化合价降低 | D. | 氢元素化合价升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
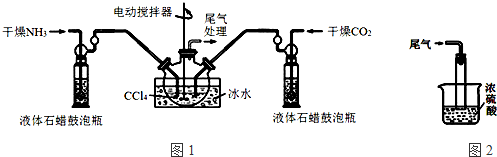
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Fe2+ | 5.8 | 8.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
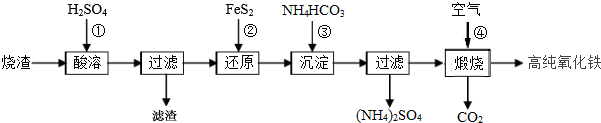
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
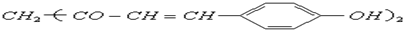 ,用它制成的试纸可以检验溶液的酸碱性.能够跟1mol该化合物起反应的Br2水溶液或H2的最大用量分别是( )
,用它制成的试纸可以检验溶液的酸碱性.能够跟1mol该化合物起反应的Br2水溶液或H2的最大用量分别是( )| A. | 3mol 3mol | B. | 3mol 5mol | C. | 6 mol 10 mol | D. | 6 mol 8 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com