
| A. |  塑料直尺 | B. |  尼龙提包 | C. |  纯羊毛手套 | D. |  塑胶地垫 |
分析 有机合成材料简称合成材料,要判断是否属于合成材料,可抓住三个特征:有机物、合成、高分子化合物,根据图示材料的种类进行分析解答即可.
解答 解:A.塑料直尺成分为塑料,塑料属于人工合成的有机高分子材料,属于合成材料,故A不选;
B.尼龙提包成分为尼龙,属于人工合成的合成纤维,属于合成材料,故B不选;
C.纯羊毛手套成分为蛋白质,经人工饲养的动物上直接取得的纺织纤维,属于天然纤维,不属于人工合成的有机高分子材料,故C选;
D.塑胶地垫属于成分为塑料,塑料属于人工合成的有机高分子材料,属于合成材料,故D不选;
故选C.
点评 本题重点考查了材料的分类,熟悉材料中的成分,能运用所学化学知识来解决实际问题是解答关键,解答时要抓住合成材料是人工合成的有机高分子材料的定义区判断,题目难度不大.


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加水稀释时.在$\frac{c(O{H}^{-})}{C({H}^{+})}$的值增大的溶液中可大量存在:MnO4-、CO32-、K+、NH4+ | |
| B. | 100℃时,将pH=2的硫酸溶液与pH=12的氢氧化钠溶液等体积混合,溶液显中性 | |
| C. | 25℃时,NaB溶液的pH=9,则c(Na+ )-c(B-)=9.9×10-6mol•L-1 | |
| D. | 将0.2mol•L-1 的一元弱酸HA溶液和0.1mol•L-1 的NaOH溶液等体积混合:2c(OH-)+c(A-)=2c(H+)+c(HA) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3水解的离子方程式:HCO3-+H2O?CO32-+H2O- | |
| B. | Ca(OH)2的电离方程式:Ca(OH)2?Ca2++2OH- | |
| C. | AgCl 的沉淀溶解平衡表达式:AgCl(s)?Ag+(aq)+CI“(aq) | |
| D. | Na2S 水解的离子方程式:S2-+2H2O?H2S+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 起始浓度 | 甲 | 乙 | 丙 |
| C(NO2)/mol•L-1 | 0.10 | 0.20 | 0.20 |
| C(SO2)/mol•L-1 | 0.10 | 0.10 | 0.20 |
| A. | 平衡时,丙中SO2的转化率大于50% | |
| B. | 当反应平衡时,乙中c(NO2)是甲中的2倍 | |
| C. | 温度升至90℃,上述反应平衡常数为$\frac{25}{26}$,则Z正反应为吸热反应 | |
| D. | 其他条件不变,若起始时向容器乙中充入0.10mol•L-lNO2和0.20mol•L-lSO2,达到平衡时c(NO)与原平衡相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑤ | B. | ②④ | C. | ①②⑤ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
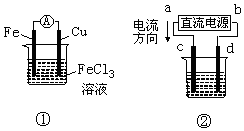
| A. | 装置①是原电池,总反应是:Cu+2Fe3+═Cu2++2Fe2+ | |
| B. | 装置①中,铁做负极,该电极反应式为:Fe3++e-═Fe2+ | |
| C. | 装置②为铁上镀铜装置c为纯铜电极 | |
| D. | 若用装置②精炼铜,则d极为粗铜,c极为纯铜,电解质溶液为CuSO4溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com