
有一种碘和氧的化合物可以称为碘酸碘,其中碘元素呈+3、+5两种价态,则这种化合物的化学式为()
| A. | I2O4 | B. | I3O5 | C. | I4O7 | D. | I4O9 |
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源: 题型:
分别将下列物质:①FeCl3②CaO③NaCl④Ca(HCO3)2⑤Na2SO3⑥K2SO4投入水中,在蒸发皿中对其溶液加热蒸干,能得到原物质的是( )
A.②③ B.③⑥ C.①④ D.⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡。
Ⅰ.已知H2A在水中存在以下平衡:H2AH++HA-,HA-H++A2-。
(1)相同浓度下,NaHA溶液的pH________(填“大于”、“小于”或“等于”) Na2A溶液的pH。
(2)某温度下,若向0.1 mol/L的NaHA溶液中逐滴滴加0.1 mol/L KOH溶液至溶液呈中性。此时该混合溶液中下列关系中,一定正确的是________。
a.c(H+)·c(OH-)=1×10-14
b.c(Na+)+c(K+)=c(HA-)+2c(A2-)
c.c(Na+)>c(K+)
d.c(Na+)+c(K+)=0.05 mol/L
(3)已知常温下H2A的钙盐(CaA)饱和溶液中存在以下平衡:
CaA(s)Ca2+(aq)+A2-(aq) ΔH>0。
①降低温度时,Ksp________(填“增大”“减小”或“不变”)。
②滴加少量浓盐酸,c(Ca2+)________(填“增大”“减小”或“不变”)。
Ⅱ.含有Cr2O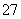 的废水毒性较大,某工厂废水中含5.00×10-3 mol·L-1的Cr2O
的废水毒性较大,某工厂废水中含5.00×10-3 mol·L-1的Cr2O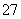 。为使废水能达标排放,作如下处理:Cr2O
。为使废水能达标排放,作如下处理:Cr2O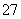
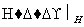 Cr3+、Fe3+石灰水,Cr(OH)3、Fe(OH)3
Cr3+、Fe3+石灰水,Cr(OH)3、Fe(OH)3
(1)该废水中加入绿矾(FeSO4·7H2O)和稀硫酸,发生反应的离子方程式为
________________________________________________________________________。
(2)欲使10 L该废水中的Cr2O 完全转化为Cr3+,理论上需要加入________g FeSO4·7H2O。
完全转化为Cr3+,理论上需要加入________g FeSO4·7H2O。
(3)若处理后的废水中残留的c(Fe3+)=2×10-13 mol·L-1,则残留的Cr3+的浓度为________。(已知:
Ksp=4.0×10-38 Ksp=6.0×10-31)
查看答案和解析>>
科目:高中化学 来源: 题型:
现有含金属元素An+的溶液,c(An+)=0.80mol•L﹣1.取该溶液10mL恰好把20mL 0.40mol•L﹣1的Na2CO3(aq)中的CO32﹣全部沉淀.已知上述10mL溶液中含此金属阳离子0.32g,则该金属的相对原子质量为()
| A. | 24 | B. | 32 | C. | 40 | D. | 64 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知由AgNO3溶液和稍过量的KI溶液制得的AgI胶体,当它跟Fe(OH)3胶体相混合时,能析出AgI和Fe(OH)3的混合沉淀,由此可知()
|
| 该AgI胶粒带正电荷 | |
| B. | 该AgI胶粒带负电荷 | |
| C. | 该AgI胶粒电泳时向阳极移动 | |
| D. | Fe(OH)3胶粒电泳时向阳极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式是()
| A. | 在碳酸氢钠溶液中加入盐酸:HCO3﹣+H+=CO2↑+H2O | |
| B. | 把金属铁放入稀硫酸中:2Fe+6H+=2Fe3++3H2↑ | |
| C. | 向氯化亚铁溶液中通入氯气:Fe2++Cl2=Fe3++2Cl﹣ | |
| D. | 钠跟水反应:Na+2H2O=Na++2OH﹣+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
碘在医药、照相、橡胶、染料、气象等许多领域都具有广泛的用途,海洋中虽然含碘的浓度相当小,每升海水中平均含碘0.06 mg,但海洋里碘的总储量仍很惊人——9.3×1010t,比陆地上要多得多 。一般生长在海底的海带含碘0.3%~0.5%,有的可达1%,比海水中碘的浓度高出十几万倍!海藻中含有丰富的碘元素(以I-形式存在)。实验室提取碘的流程如下:
。一般生长在海底的海带含碘0.3%~0.5%,有的可达1%,比海水中碘的浓度高出十几万倍!海藻中含有丰富的碘元素(以I-形式存在)。实验室提取碘的流程如下:
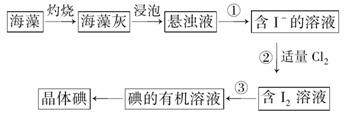
(1)在虚线框内画出实验操作①的仪器装置示意图。实验操作③的名称是__________,所用主要仪器名称为__________________。
 |
说明:实验装置中仪器用下面方法表示。铁架台、连接胶管等不必画出,如需加热,在仪器下方用“△”表示。下列图示均为玻璃仪器,应标清液面或固体可视界面。
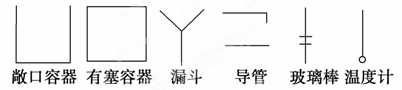
(2)提取碘的过程中,可供选择的有机试剂是____________(填序号)。
A.酒精(沸点78 ℃) B .四氯化碳(沸点77 ℃)
.四氯化碳(沸点77 ℃)
C.甘油(沸点290 ℃) D.苯(沸点80 ℃)
(3)在操作②中,溶液中生成少量ICl,为消耗此杂质,使碘全部游离出来,应加入适量________(填序号)溶液,反应的离子方程式为____________。
A.KIO3 B.HClO C.KI D.Br2
(4)为使从含碘有机溶液中提取碘并回收溶剂, 采用水浴加热蒸馏(如图所示)。请指出图中实验装置中错误之处(有处填几处,下列空白可不填满,也可补充)。
采用水浴加热蒸馏(如图所示)。请指出图中实验装置中错误之处(有处填几处,下列空白可不填满,也可补充)。
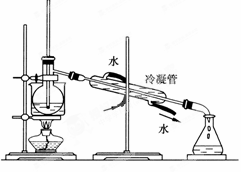
①______ ,
②__ ,
③___________ __ ,
__ ,
④_________________ 。
(5)实验中使用水浴的原因是____________,最后晶体碘聚集在_____(填仪器名称)中。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com