
【题目】1,4-环己二醇可通过下列路线合成(某些反应的反应物和反应条件未列出):
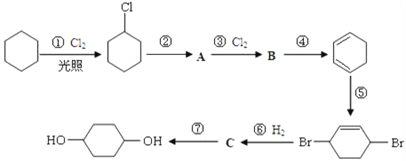
(1)写出反应④、⑦的化学方程式:
④______________________________________________________________;
⑦______________________________________________________________。
(2)②的反应类型是____________,上述七个反应中属于加成反应的有____________(填反应序号)。
(3)反应⑤中可能产生一定量的副产物,其可能的结构简式为_________________。
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,某容器中各微粒在反应前后变化的示意图如下,其中●和○代表不同元素的原子。

关于此反应的说法不正确的是
A. 反应物总能量一定低于生成物总能量 B. 一定属于可逆反应
C. 一定有非极性共价键断裂 D. 一定属于氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知一定条件下断裂或形成某些化学键的能量关系如下表:
断裂或形成的化学键 | 能量数据 |
断裂1 mol H2分子中的化学键 | 吸收能量436 kJ |
断裂1 mol Cl2分子中的化学键 | 吸收能量243 kJ |
形成1 mol HCl分子中的化学键 | 释放能量431 kJ |
对于反应:H2(g)+Cl2(g)===2HCl(g),下列说法正确的是
A. 该反应的反应热ΔH>0
B. 生成1 mol HCl时反应放热431 kJ
C. 氢气分子中的化学键比氯气分子中的化学键更牢固
D. 相同条件下,氢气分子具有的能量高于氯气分子具有的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在KI溶液中存在下列平衡:I2(aq)+I-(aq)![]() I3- (aq)。某I2、KI混合溶液中I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是
I3- (aq)。某I2、KI混合溶液中I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是

A. 反应I2(aq)+I-(aq) ![]() I3- (aq)的ΔH>0
I3- (aq)的ΔH>0
B. 若温度为T1、T2时,反应的平衡常数分别为K1、K2,则K1<K2
C. 若反应进行到状态D时,一定有v(正) > v(逆)
D. 状态A与状态B相比,状态A的c(I2)大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的固体![]() 置于容积不变的密闭容器中(装有少量
置于容积不变的密闭容器中(装有少量![]() ,某温度下发生反应:
,某温度下发生反应:![]()
![]()
![]() ,
,![]()
![]()
![]() ,反应经过10 min达到平衡,测得c(SO3)=0.4mol/L,c(SO2)=0.1mol/L,则下列叙述中不正确的是
,反应经过10 min达到平衡,测得c(SO3)=0.4mol/L,c(SO2)=0.1mol/L,则下列叙述中不正确的是
A. 化学反应速率![]()
B. ![]() 的分解率为20%
的分解率为20%
C. 在这10 min内的平均反应速率![]()
D. 容器里气体的密度为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国明代《本草纲目》中收载药物1892种,其中“烧酒”条目下写道:“自元时始创其法,用浓酒和糟入甑,蒸令气上……其清如水,味极浓烈,盖酒露也。”这里所用的“法”是指 ( )
A.萃取B.蒸馏C.渗析D.干馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA,下列说法正确的是
A. 用惰性电极电解KOH溶液,若阳极产生5.6L气体,则电路中通过0.5NA电子
B. 常温常压下.4.6gNO2气体所含的分子数为0.1NA
C. 7.8gNa2O2与足量的水(H218O)反应生成的氧气所含的中子数为NA
D. 100g46%甲酸(HCOOH)水溶液所含的氧原子数为5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“纳米材料”是粒子直径为1~100 nm(纳米)的材料,纳米碳就是其中的一种。若将纳米碳均匀地分散到蒸馏水中,所形成的物质( )
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸⑤能透过半透膜 ⑥加入CuCl2,会析出沉淀 ⑦带正电荷
A.①④⑥B.②③④C.②③⑤D.②③④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com