
Li﹣Al/FeS电池是一种正在开发的车载电池,该电池中正极的电极反应式为:2Li++FeS+2e﹣=Li2S+Fe.有关该电池的下列说法中,正确的是()
A. Li﹣Al在电池中作为负极材料,该材料中Li的化合价为+1价
B. 该电池的电池反应式为:2Li+FeS=Li2S+Fe
C. 负极的电极反应式为Al﹣3e﹣=Al3+
D. 充电时,阴极发生的电极反应式为:Li2S+Fe﹣2e﹣=2Li++FeS
考点: 电极反应和电池反应方程式;化学电源新型电池.
分析: Li和Al都属于金属,合金中Li较Al活泼,根据正极反应式知,原电池的电极材料Li﹣Al/FeS,判断出负极材料为Li,发生反应为:Li﹣e﹣=Li+,又知该电池中正极的电极反应式为:2Li++FeS+2e﹣=Li2S+Fe,所以电池反应为:2Li+FeS=Li2S+Fe,充电时为电解池原理,阴极发生还原反应,正确的反应式是2Li++2e﹣=2Li.
解答: 解:A、Li和Al都属于金属,所以Li﹣Al应该属于合金而不是化合物,因此化合价为0价,故A错误;
B、根据正极反应2Li++FeS+2e﹣=Li2S+Fe与负极反应2Li﹣2e﹣=2Li+相加可得反应的电池反应式为:2Li+FeS=Li2S+Fe,故B正确;
C、由正极反应式知负极应该是Li失去电子而不是Al,故C错误;
D、充电时为电解池原理,阴极发生还原反应,正确的反应式是2Li++2e﹣=2Li,故D错误;
故选:B.
点评: 本题涵盖电解池和原电池的主体内容,涉及电极判断与电极反应式书写等问题,做题时注意从氧化还原的角度判断原电池的正负极以及电极方程式的书写,本题中难点和易错点为电极方程式的书写.


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
有A、B、C、D、E 5种元素,它们的核电荷数依次增大,且都小于20.其中只有C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1、B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半.请回答下列问题.
(1)A是 ,B是 ,C是 ,E是 .
(2)B在周期表中位于 区.
(3)写出C元素基态原子核外电子排布式, .
(4)用轨道表示式表示D元素原子的价电子构型 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子可以大量共存的是( )
A. Na+、Ba2+、SO42﹣、Cl﹣ B. H+、Ag+、Cl﹣、NO3﹣
C. K+、H+、CO32﹣、Cl﹣ D. Cu2+、Fe3+、Cl﹣、NO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中可能有下列阴离子中的一种或几种:SO42﹣、CO32﹣、Cl﹣、OH﹣.
(1)当溶液中有大量H+存在时,则不可能有 存在,发生反应的离子方程式 ;
当溶液中有大量Ba2+存在时,则不可能有 存在,发生反应的离子方程式 ;
(3)检验某溶液中是否存在SO42﹣的试剂为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下,下列溶液的离子浓度关系式正确的是()
A. pH=5的H2S溶液中,c(H+)=c(HS﹣)=1×10﹣5 mol•L﹣1
B. pH相同的①CH3COONa、②NaHCO3、③NaClO三种溶液的c(Na+):①>②>③
C. pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
D. pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c(H+)=c(OH﹣)+c(HC2O4﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
在BaSO4饱和溶液中,加入Na2SO4(s),达平衡时()
A. c(Ba2+)=c(SO42﹣)
B. c(Ba2+)≠c(SO42﹣),c(Ba2+)•c(SO42﹣)=Ksp(BaSO4)
C. c(Ba2+)=c(SO42﹣)=[Ksp(BaSO4)]1/2
D. c(Ba2+)≠c(SO42﹣),c(Ba2+)•c(SO42﹣)≠Ksp(BaSO4)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中粒子的物质的量浓度关系正确的是()
A. 0.1mol/L NaHCO3溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32﹣)>c(HCO3﹣)>c(OH﹣)
B. 20mL 0.1mol/L CH3COONa溶液与10mL 0.1mol/L HCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO﹣)>c(Cl﹣)>c(CH3COOH)>c(H+)
C. 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl﹣)+c(H+)>c(NH4+)+c(OH﹣)
D. 0.1mol/L CH3COOH溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c(OH﹣)>c(H+)+c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
类推的思维方法在化学学习与研究中有时会产生错误结论,因此类推的结论最终要经过实践的检验,才能确定其正确与否,下列几种类推结论中,错误的是()
①钠与水反应生成NaOH和H2;所有金属与水反应都生成碱和H2
②铁露置在空气中一段时间后就会生锈;性质更活泼的铝不能稳定存在于空气中
③化合物NaCl的焰色为黄色;Na2CO3的焰色也为黄色
④密度为1.1g•cm﹣3与密度为1.2g•cm﹣3的NaCl溶液等体积混合,所得NaCl溶液的密度介于1.1g•cm﹣3与1.2g•cm﹣3之间;NaK合金的熔点应介于Na和K熔点之间.
A. ①② B. ①④ C. ①②③④ D. ①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,下图烧杯中各盛有25mL的溶液.
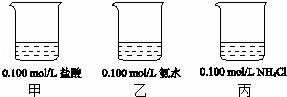
(1)甲溶液pH=1.
(2)若将甲溶液全部倒入乙中,所得的混合溶液的pH(填“>”、“<”或“=”) 丙溶液的pH.
(3)若将乙溶液全部倒入丙中,所得的混合溶液pH>7,所得溶液中离子浓度大小顺序是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com