
【题目】75%的酒精、“84”消毒液、双氧水等化学品均是抗疫期间常用的消毒剂。下列有关“84”消毒液(NaClO和NaCl混合溶液)的叙述正确的是( )
A.该溶液中,H+、![]() 、
、![]() 、I-可以大量共存
、I-可以大量共存
B.该溶液中,Ag+、K+、![]() 、CH3CH2OH可以大量共存
、CH3CH2OH可以大量共存
C.向该溶液中加入浓盐酸,会产生黄绿色气体Cl2
D.向该溶液中滴入少量FeSO4溶液的离子方程式为:2Fe2++ClO-+2H+=Cl-+2Fe3++H2O
【答案】C
【解析】
A.ClO-具有强氧化性,酸性条件下能与溶液中I-发生氧化还原反应,在溶液中不能大量共存,故A错误;
B.在溶液中Cl-与Ag+生成AgCl沉淀,另ClO-具有强氧化性,能将CH3CH2OH氧化降低消毒效果,不能大量共存,故B错误;
C.ClO-具有强氧化性,能与浓盐酸发生氧化还原反应生成黄绿色气体氯气,反应的化学方程式为Cl-+ClO-+2H+=Cl2↑+ H2O,故C正确;
D.ClO-在溶液中水解使溶液呈碱性,碱性条件下,ClO-与Fe2+发生氧化还原反应Cl-、Fe(OH)3和H2O,反应离子方程式为:2Fe2++ClO-+4OH+ H2O -=Cl-+2Fe(OH)3↓,故D错误;
故选C。


科目:高中化学 来源: 题型:
【题目】如下图,CPAE是蜂胶的主要活性成分,也可由咖啡酸合成.下列说法不正确的是

A.咖啡酸分子中所有碳原子可能处在同一个平面上
B.1molCPAE与足量的溴水反应,最多消耗3molBr2
C.1mol苯乙醇在O2中完全燃烧,需消耗10molO2
D.1molCPAE与足量的NaOH溶液反应,最多消耗3molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分氧化的铁铜合金样品(氧化产物为Fe2O3、CuO)共5.76g,经如图处理:

(1)滤渣成分为__,滤液A中含有的阳离子为__。
(2)样品中铁元素的质量分数为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D是中学化学中常见的四种不同粒子,它们之间存在如图所示的转化关系(反应条件已经略去):
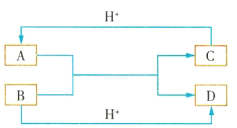
(1)若A、B、C、D均是10电子粒子,请写出A、D的化学式:A___;D___。
(2)若A和C均是18电子粒子,且A为阴离子,B和D均是10电子粒子,则A与B在溶液中反应的离子方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为比较Fe3+和Cu2+对H2O2分解的催化效果,某体学研究小组的同学分别设计了图甲、乙所示的实验。请回答相关问题:

(1)定性比较:图甲可通过观察_____,定性比较得出结论。有同学提出将CuSO4改为CuCl2更合理一些,其理由是______。
(2)定量比较:如图乙所示,实验时均以生成40 mL气体为标准,其他可能影响实验的因素均已忽略。检查该装置气密性的方法是________,实验中需要测量的数据是_______。
(3)将0.10 mol MnO2粉末加入到50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示。
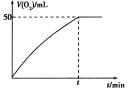
①写出H2O2在MnO2作用下发生反应的化学方程式:_______。
②H2O2的初始物质的量浓度为________。(保留两位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】央视报道《王者归“铼”》:中国发现超级金属“铼”,飞机火箭上天全靠它,有望打破美国垄断。
(1)铼(Re)被称为类锰元素,与锰的外围电子结构数相同,已知Mn的外围电子排布式为3d54s2,写出75Re的外围电子排布式:______,其最高价氧化物的化学式为_______。
(2)铢合金可作为醇脱氢反应的催化剂:CH3OH![]() HCHO+H2↑,上述反应两种有机物中碳原子的杂化形式分别是______和_______。C、H、O三种元素中,电负性最大的是______(填元素符号)。
HCHO+H2↑,上述反应两种有机物中碳原子的杂化形式分别是______和_______。C、H、O三种元素中,电负性最大的是______(填元素符号)。
(3)实验中常用过硫酸盐氧化法测定钢铁中锰的含量,反应原理为2Mn2++5S2O82-+8H2O![]() 2MnO4-+10SO42-+16H+。已知H2S2O8的结构简式如图所示。
2MnO4-+10SO42-+16H+。已知H2S2O8的结构简式如图所示。
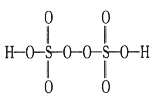
上述反应中S2O82-断裂的共价键类型为___(填“σ键”或“π键”),每生成0.3molMnO4-,过硫酸根中断裂的共价键数目为_____NA。
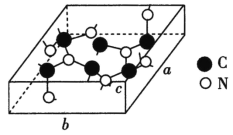
(4)科学家研制出一种新型的超硬材料,类似于金刚石的结构,但硬度比金刚石大,该晶体元素组成为C和N,其晶胞如图所示(图示原子都包含在晶胞内),则该晶胞所含氮原子的个数为____。已知晶胞参数分别为a nm、b nm、c nm,,该晶体的摩尔质量为Mg·mol-1,密度为ρg·cm-3,则阿伏加德罗常数的数值为___(用含a、b、c、ρ、M的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.除最外层外,原子中各电子层上的电子数均已达到2n2个
B.最外层只有1个电子的原子失去1个电子后都变成了稀有气体元素原子的电子层结构
C.某原子M层上的电子数为L层的3倍
D.某简单离子L层上的电子数为K层的4倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水硫酸铜(CuSO4)为白色或灰白色粉末。其水溶液显蓝色,呈弱酸性。可用作杀菌剂和电解精炼铜时的电解液。某化学课外活动小组通过设计硫酸铜受热分解的探究实验,测定气体产物的成分(已知硫酸铜完全分解,固体产物仅含CuO)。实验装置如图所示,回答下列问题

(1)实验前需进行的操作是_________,仪器a的名称是_____,加热时试管外壁必须干燥,要先均匀加热,再集中加热,其目的是__________。
(2)实验结束时根据f中量筒是否收集到水,确定气体产物中有无_______(填化学式)。
(3)装置c的作用是_________。
(4)装置d中的化学方程式为____,_____。有小组成员建议在装置d后增加连接一个干燥管,其原因是_______。
(5)按完善装置的实验结束前后测得相关数据如下:(填化学式)。
实验前无水硫酸铜的质量/g | 实验后装置d增加的质量/g | 量筒中水的体积折算成标准状况下气体的体积/mL |
6.4 | 2.56 | 224 |
通过计算,写出CuSO4受强热分解的化学方程式:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不同温度下,水溶液中![]() 的物质的量浓度和
的物质的量浓度和![]() 的物质的量浓度的关系如图所示.下列说法不正确的是
的物质的量浓度的关系如图所示.下列说法不正确的是![]()

A.M点和N点对应的溶液均呈中性
B.![]() 时,P点对应溶液中,水电离出来的
时,P点对应溶液中,水电离出来的![]() 可能为
可能为![]() 或
或![]()
C.![]() 时,
时,![]() 的NaOH溶液与
的NaOH溶液与![]() 的稀
的稀![]() 等体积混合,所得溶液的
等体积混合,所得溶液的![]()
D.向某溶液中加入酸或碱,均可以使该溶液从M点转化为N点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com