
���� ��1���ٵõ��ӣ����ϼ۽��͵ķ�Ӧ������������
�ڸ��ݻ��ϼ�����������ȡ�ԭ���غ�����ƽ��
��2�����������ӻ��Cr2O72-�����Է�ˮ��Ӧ��������Ӧ�����ӷ���ʽ��Cr2O72-+6Fe2++14H+�T2Cr3++6Fe3++7H2O����ϵ缫����ʽFe-2e-�TFe2+���㣻
�ڸ����ܶȻ����㣻
��3���ټ���һ���� Na2S2O3 ��Һ��������Ӧ2S2O32-+I2�TS4O62-+2I-��ʹI2��ԭΪI-��
����ͼʾ������pH��1��3ʱ��ClO2-��I-�������ɵ�I2����۽���ٴγ�����ɫ�����ݻ��ϼ�����������ȡ�ԭ���غ�͵���غ�����ƽ��
�۸��ݹ�ϵʽClO2��I-��S2O32-�ȼ����ClO2�����ʵ�����Ȼ���ټ����Ũ�ȣ�
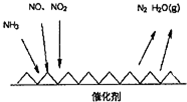
��� �⣺��1������ͼ��֪SCR������NH3��NO��NO2��Ӧ����ΪN2��ˮ����������ΪNO��NO2��
�ʴ�Ϊ��NO��NO2��
��NH3�е��Ļ��ϼ���-3�����ߵ�0�ۣ�һ��NH3ʧȥ3�����ӣ�NO2�е��Ļ��ϼ���+4�۽��͵�0�ۣ�һ��NO2�õ�4�����ӣ�NO�е��Ļ��ϼ���+2�۽��͵�0�ۣ�һ��NO�õ�2�����ӣ���NO2��NO�����ʵ���֮��Ϊ1��1ʱ��ת�Ƶ��ӵ���С������Ϊ6����������غ��֪����ʽΪ��2NH3+NO+NO2$\frac{Fe}{��}$2N2+3H2O��
�ʴ�Ϊ��2NH3+NO+NO2$\frac{Fe}{��}$2N2+3H2O��
��2�����������ӻ��Cr2O72-�����Է�ˮ��Ӧ��������Ӧ�����ӷ���ʽ��Cr2O72-+6Fe2++14H+�T2Cr3++6Fe3++7H2O�������缫����ʽFe-2e-�TFe2+����
Cr2O72-��6Fe2+��12mol���ӣ�1mol Cr2O72-��ȫ����Cr��0H��3���������·ͨ�����ӵ����ʵ���Ϊ12mol��
�ʴ�Ϊ��12��
����Һ��pH=6����c��OH-��=10-8mol•L-1����c3��OH-����c��Cr3+��=Ksp=10-32��c��Cr3+��=10-8mol•L-1��10-5mol•L-1����ֱ���ŷţ�
�ʴ�Ϊ���ܣ�
��3���ټ���һ���� Na2S2O3 ��Һ��������ӦΪ��2S2O32-+I2�TS4O62-+2I-��ʹI2��ԭΪI-������ɫ����ʧ���ʴ�Ϊ����ɫ��ʧ��������ڲ���ɫ��
����ͼʾ������pH��1��3ʱ��ClO2-��I-�������ɵ�I2��ClO2-���ȵĻ��ϼ���+3�۽��͵�-1�ۣ�һ��ClO2-�õ�4�����ӣ���Ļ��ϼ���-1�����ߵ�0�ۣ�һ��I-ʧȥ1�����ӣ�ת�Ƶ��ӵ���С������Ϊ4����������غ㡢����غ��֪���ӷ���ʽΪ��ClO2-+4I-+4H+=Cl-+2I2+2H2O��
�ʴ�Ϊ��ClO2-+4I-+4H+=Cl-+2I2+2H2O��
��ClO2 ��I-��S2O32-
1 1
1.0��10-5mol 1.0��10-3 mol/L��0.01L
m��ClO2��=n��ClO2����M��ClO2��=1.0��10-5mol��67.5��103mg•mol-1=0.675mg
����ˮ�������Ϊ1.0L������ ClO2 ��Ũ��Ϊ$\frac{0.675mg}{1L}$=0.675 mg•L-1��
�ʴ�Ϊ��0.675��
���� ������Ҫ������������ԭ��Ӧ�����ӷ���ʽʽ����д�Լ���ѧ���㣬�Ѷ��еȣ�ע������ʵ��ԭ���͵��ӵ�ʧ��ƽ�ķ�����


 ȫ�ܲ����ĩС״Ԫϵ�д�
ȫ�ܲ����ĩС״Ԫϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1molCl2�����������۷�Ӧ����Ӧת�Ƶ��ӵ���ĿΪ3NA | |
| B�� | ����ʱ������Zn��Ũ���ᷴӦ������2mol���壬ת�Ƶ�����Ϊ4NA | |
| C�� | 7.8gNa2O2������ˮ��Ӧʱת�Ƶ�����ĿΪ0.2NA | |
| D�� | 1mol��������������ú��ڱ�״���µ����Ϊ22.4L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 | B�� | l-a | C�� | 2-lga | D�� | 3-lga |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 50mL18.4mol/LŨ����������ͭ�ȷ�Ӧ������SO2���ӵ���ĿΪ0.46NA | |
| B�� | ij�ܱ�����ʢ��0.1mol N2��0.3mol H2����һ�������³�ַ�Ӧ��ת�Ƶ��ӵ���ĿΪ0 6NA | |
| C�� | ����CO2��O2��ɵĻ�����й���NA�����ӣ������е���ԭ����Ϊ2 NA | |
| D�� | �����£�1L 0�� 1 mol/L NH4NO3��Һ�е���ԭ����Ϊ0.4 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�Ӱ뾶��W��Z��Y | |
| B�� | ��ҵ��ͨ�����Y����ˮ�����Ʊ�Y�ĵ��� | |
| C�� | ����������Ӧˮ��������ԣ�W��Z��X | |
| D�� | ��Ԫ�طֱ���X��Y��Z��W�γɵĻ����ﶼ��ֹһ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢ� | B�� | �٢ۢ� | C�� | �ۢܢ� | D�� | �٢ۢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com