
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将某有机物与溴的四氯化碳溶液混合 | 溶液褪色 | 该有机物中必定含有碳碳双键 |
| B | 向亚硫酸钠溶液中滴加硝酸钡和稀硝酸 | 产生白色沉淀 | 亚硫酸钠溶液已变质 |
| C | 向酸性高锰酸钾溶液中滴加双氧水 | 紫色褪去,产生气泡 | H2O2具有还原性 |
| D | 向油脂皂化反应后的溶液中滴入酚酞 | 溶液不变红 | 油脂已经完全皂化 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.碳碳不饱和键、醛基都能与溴发生反应;
B.亚硫酸钠能被硝酸氧化生成硫酸根离子,硫酸根离子和钡离子反应生成BaSO4沉淀;
C.酸性高锰酸钾溶液褪色,证明H2O2具有还原性;
D.高级脂肪酸钠溶液呈碱性.
解答 解:A.C=C、C≡C三键、醛基等都可以使溴的四氯化碳溶液褪色,故A错误;
B.亚硫酸钠能被硝酸氧化生成硫酸根离子,硫酸根离子和钡离子反应生成BaSO4沉淀,所以该白色沉淀是硫酸钡,不一定变质,故B错误;
C.H202具有还原性,高锰酸钾溶液紫红色褪去,离子方程式为2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑,故C正确;
D.高级脂肪酸钠溶液呈碱性,向油脂皂化反应后的溶液中滴入酚酞,溶液不变红,说明油脂未水解,故D错误.
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及物质的检验以及氧化还原反应等,侧重实验基本操作和实验原理的考查,注意装置的作用及实验的操作性、评价性分析,题目难度不大.


科目:高中化学 来源: 题型:填空题
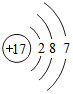 .
.查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Z、W、Q、X、Y原子半径依次减小 | |
| B. | W最高价氧化物对应水化物一定能溶于Z最高价氧化物对应水化物的溶液中 | |
| C. | Y与Q形成化合物在常温下一定为气态 | |
| D. | Z、Q元素的单质都可以将X元素的单质从其氧化物中置换出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
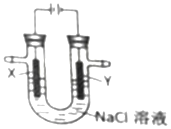
| A. | X电极为阴极 | B. | Y电极为负极 | ||
| C. | X电极表面发生氧化反应 | D. | Y电极表面有氯气生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
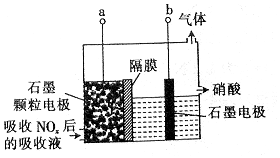
| A. | 吸收NOx的过程涉及氧化还原反应 | |
| B. | 石墨电极为颗粒状,可增大接触面积,提高电解效率 | |
| C. | 当b极上产生2.8 L(标准状况)H2时,转移的电子数为0.5NA(设NA为阿伏加德罗常数的数值) | |
| D. | a极的电极反应式为HNO2-2e-+H2O═3H++NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12gC与16gO2所具有的总能量一定高于28gCO所具有的能量 | |
| B. | 56gCO所具有的能量大于88gCO2所具有的能量 | |
| C. | 12gC和32gO2所具有的总能量大于44gCO2所具有的能量 | |
| D. | 将一定质量的碳燃烧,生成CO2比生成CO时放出的热量多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 向甲、乙、丙三个恒容密闭容器中分别充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).相关数据如表,反应过程中C的浓度随时间变化关系如图.下列说法正确的是( )
向甲、乙、丙三个恒容密闭容器中分别充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).相关数据如表,反应过程中C的浓度随时间变化关系如图.下列说法正确的是( )| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | 1.0L |
| 温度/℃ | T1 | T2 | T2 |
| 反应物 起始量 | 1.5 mol A 0.5 mol B | 1.5 mol A 0.5 mol B | 6 mol A 2 mol B |
| A. | T1>T2,x=1 | |
| B. | T2℃时,该反应的平衡常数为0.8 | |
| C. | A的平衡转化率a(甲):a(乙)=2:3 | |
| D. | 15~20min内C的平均反应速率v(乙)<v(丙) |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高一上第一次月考化学试卷(解析版) 题型:选择题
某10% NaOH溶液,加热蒸发掉100g水后得到80mL 20%的溶液,则该20% NaOH溶液的物质的量浓度为( )
A.6.25mol·L-1 B.12.5mol·L-1 C.7mol·L-1 D.7.5mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com