
| A、2g | B、4g |
| C、10g | D、12g |
| 2.8L |
| 22.4L/mol |
| 65g×0.125mol |
| 1mol |
| 54g×0.125mol |
| 3mol |


科目:高中化学 来源: 题型:
| A、四种元素形成的简单离子半径按照D、C、B、A的顺序逐渐减小 |
| B、A与其它元素形成的二元化合物的晶体类型相同 |
| C、Z气体通入BaCl2溶液中无现象,再滴入FeCl3溶液则可看到有沉淀产生 |
| D、X的水溶液和Y的水溶液一种呈酸性另一种呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
 )是最简单的芳香胺,暴露于空气中变为棕色,该变化最有可能与苯胺具有
)是最简单的芳香胺,暴露于空气中变为棕色,该变化最有可能与苯胺具有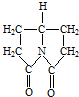 写出该有机物在酸催化下水解产物的结构简式
写出该有机物在酸催化下水解产物的结构简式查看答案和解析>>
科目:高中化学 来源: 题型:
 向含有一定量盐酸和少量MgSO4的混合溶液中逐滴加入Ba(OH)2溶液,产生沉淀的质量m克与加入Ba(OH)2的物质的量n之间的关系如图所示,下列说法正确的是( )
向含有一定量盐酸和少量MgSO4的混合溶液中逐滴加入Ba(OH)2溶液,产生沉淀的质量m克与加入Ba(OH)2的物质的量n之间的关系如图所示,下列说法正确的是( )| A、a→b时的沉淀成分为BaSO4与Mg(OH)2 |
| B、原混合溶液中:n(HCl)=2mol |
| C、c点时的溶液中c(Cl-)>c(OH-)>c(Ba2+) |
| D、b→c时发生的离子反应为H++OH-=H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入少量金属Na,平衡①左移,平衡②右移,溶液中c(HSO3-)增大 | ||||||||
B、加入少量Na2SO3固体,则c(H+)+c(Na+)=c(HSO3-)+c(OH-)+
| ||||||||
C、加入少量NaOH溶液,
| ||||||||
| D、加入氨水至中性,则c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、X分子中含有手性碳原子 |
| B、X可发生氧化、消去、取代等反应 |
| C、X既能与盐酸反应,又能与NaOH溶液反应 |
| D、1mol X与H2反应,最多消耗4mol H2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com