
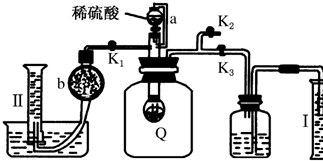
 为测定保存在干燥环境中已部分变质的过氧化钠样品(只有一种杂质)的纯度,设计了如图所示的实验装置,图中Q为弹性良好的气球,称取一定量的样品放入其中,按图安装好仪器,打开漏斗的活塞,将稀硫酸滴入气球中.
为测定保存在干燥环境中已部分变质的过氧化钠样品(只有一种杂质)的纯度,设计了如图所示的实验装置,图中Q为弹性良好的气球,称取一定量的样品放入其中,按图安装好仪器,打开漏斗的活塞,将稀硫酸滴入气球中.| 2mol×y×10-3L |
| 22.4L |
| 1mol×(x-y)×10-3L |
| 22.4L |
| m(Na2O2) |
| m(Na2O2)+m(Na2CO3) |
| 78y |
| 53x+25y |
| 78y |
| 53x+25y |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、Zn为正极,Cu为负极,CuCl2溶液作电解质溶液 |
| B、Cu为正极,Zn为负极,稀H2SO4作电解质溶液 |
| C、Cu为正极,Zn为负极,CuSO4溶液作电解质溶液 |
| D、Fe为正极,Zn为负极,CuCl2溶液作电解质溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、赤铁矿的主要成分是Fe3O4 |
| B、铁矿石的主要成分与铁锈的主要成分相同 |
| C、磁铁矿粉末溶于盐酸后,加入KSCN溶液,溶液变血红色 |
| D、FeO俗称铁红 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| HCl |
| Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
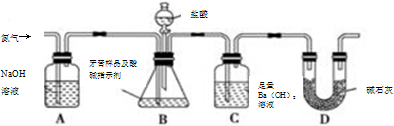
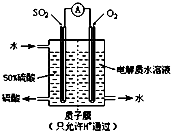 研究NO2、SO2、CO等大气污染气体的测量及处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的测量及处理具有重要意义.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com