
【题目】探究2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+10CO2↑+8H2O反应速率的影响因素,有关实验数据如下表所示:下列说法不正确的是( )
实验编号 | 温度 | 催化剂用量(g) | 酸性KMnO4溶液 | H2C2O4溶液 | KMnO4溶液褪色平均时间 min | ||
体积(mL) | 浓度mol·L-1 | 体积(mL) | 浓度 mol·L-1 | ||||
1 | 25 | 0.5 | 4 | 0.1 | 8 | 0.2 | 12.7 |
2 | 80 | 0.5 | 4 | 0.1 | 8 | 0.2 | a |
3 | 25 | 0.5 | 4 | 0.01 | 8 | 0.2 | 6.7 |
4 | 25 | 0 | 4 | 0.01 | 8 | 0.2 | b |
A. a<12.7,b>6.7
B. 用KMnO4表示该反应速率,v(实验3)<v(实验1)
C. 用H2C2O4表示该反应速率,v(实验1)约为7.87×10-5 mol·L-1·min-1
D. 可通过比较收集相同体积CO2所消耗的时间来判断反应速率快慢
【答案】C
【解析】
A. 温度越高反应速率越快,催化剂可加快反应速率;
B. 实验编号1和3对照,单一变量控制法分析作答;
C.结合![]() =
= ![]() 及速率之比等于化学计量数之比计算;
及速率之比等于化学计量数之比计算;
D.比较收集相同体积CO2所消耗的时间,可知反应的快慢。
A. 温度越高反应速率越快,催化剂可加快反应速率,则a<12.7,b>6.7,故A项正确;
B. 实验编号1和3对照发现,只有高锰酸钾的浓度不同,且实验1中其高锰酸钾的浓度大,则反应速率:v(实验3)<v(实验1),故B项正确;
C. 实验1中,高锰酸钾的用量少,根据关系式2KMnO4![]() 5H2C2O4可知,消耗的H2C2O4的物质的量浓度为
5H2C2O4可知,消耗的H2C2O4的物质的量浓度为![]() =
=![]() mol/L,则用H2C2O4表示实验1的反应速率时,其值为
mol/L,则用H2C2O4表示实验1的反应速率时,其值为![]() ≈ 6.56×l03 molL1min1,故C项错误;
≈ 6.56×l03 molL1min1,故C项错误;
D. 比较收集相同体积CO2所消耗的时间,可知反应速率大小,进而可判断反应速率快慢,故D项正确;
答案选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】苯甲酸钠(![]() ,缩写为NaA)可用作饮料的防腐剂。研究表明苯甲酸(HA)的抑菌能力显著高于A–。已知25 ℃时,HA的Ka=6.25×10–5,H2CO3的Ka1=4.17×10–7,Ka2=4.90×10–11。在生产碳酸饮料的过程中,除了添加NaA外,还需加压充入CO2气体。下列说法正确的是(温度为25 ℃,不考虑饮料中其他成分)
,缩写为NaA)可用作饮料的防腐剂。研究表明苯甲酸(HA)的抑菌能力显著高于A–。已知25 ℃时,HA的Ka=6.25×10–5,H2CO3的Ka1=4.17×10–7,Ka2=4.90×10–11。在生产碳酸饮料的过程中,除了添加NaA外,还需加压充入CO2气体。下列说法正确的是(温度为25 ℃,不考虑饮料中其他成分)
A. 相比于未充CO2的饮料,碳酸饮料的抑菌能力较低
B. 提高CO2充气压力,饮料中c(A–)不变
C. 当pH为5.0时,饮料中![]() =0.16
=0.16
D. 碳酸饮料中各种粒子的浓度关系为:c(H+)=c(![]() )+c(
)+c(![]() )+c(OH–)–c(HA)
)+c(OH–)–c(HA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值下列有关叙述正确的是
A. 常温常压下, 30 g乙烷中所含的极性共价键数为6NA
B. 0.1mol Fe与足量盐酸反应,转移的电子数为0.3NA
C. 0.1 mol![]() Sr原子中含中子数为3.8NA
Sr原子中含中子数为3.8NA
D. 0.1mol·L-1的NH4NO3溶液中含有的氮原子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2A为二元弱酸。20℃时,配制一组c(H2A)+c(HA﹣)+c(A2﹣)=0.100molL﹣1的H2A和NaOH的混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如下图所示。下列指定溶液中微粒的物质的量浓度关系一定正确的是( )
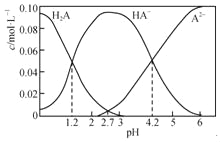
A. H2A的Ka1=10﹣1.2
B. pH=4.2的溶液中:c(HA﹣)=c(A2﹣)=0.050 molL﹣1
C. pH=7的溶液中:c(Na+)>2c(A2﹣)+c(H+)
D. c(Na+)=0.150 molL﹣1的溶液中:2c(OH﹣)+c(HA﹣)+3c(H2A)=2c(H+)+c(A2﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常用的漂白粉是次氯酸钙,氯化钙和氢氧化钙所组成的水合复盐,是由Cl2与消石灰制成的。有关反应如下:2Cl2+3Ca(OH)2=Ca(ClO)2·CaCl2·Ca(OH)2·H2O+H2O
(1)漂白粉的有效成分是________________________________________;
(2)漂白粉在潮湿的空气中放置会慢慢失效,有关反应的化学方程式为: _______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组利用下列装置迅速制备少量氯气。提供的试剂有:浓盐酸、饱和食盐水、氢氧化钠溶液、高锰酸钾固体。(2KMnO4+16HCl(浓)→2KCl+2MnCl2+5Cl2↑+8H2O)

试回答:
(1)装置H中盛放的试剂是_________________________________________。
(2)尾气处理时关闭弹簧夹a和弹簧夹________________,打开弹簧夹________________。
(3)处理尾气时,发生反应的化学方程式是____________________________。
(4)从装置G中出来的Cl2中含有________________气体,可用________________试剂除去。
(5)标出该反应的电子转移方向和数目:2KMnO4+16HCl(浓)→2KCl+2MnCl2+5Cl2↑+8H2O_______,此反应中的氧化剂是________,被氧化的元素是________,若参加反应的氧化剂的物质的量是1mol,则产生的氯气在标准状况下的体积为________,被氧化的物质的物质的量为________(有单位的需注明单位)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化锗被广泛用于制作高纯金属锗、锗化合物、化工催化剂及医药工业,某工厂用褐煤烟灰(主要成分C、GeO2,还有少量Al2O3和SiO2)为原料制备GeO2,其流程如下:
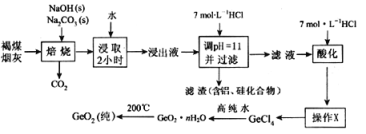
已知:GeO2难溶于水,不跟水反应,是以酸性为主的两性氧化物,溶于强碱溶液生成锗酸盐,与浓盐酸生成GeCl4(GeCl4的沸点是83.1℃)
(1)用水浸取焙烧物2小时的目的是____________________,操作“X”的名称为________,该操作除了冷凝管、铁架台、牛角管、锥形瓶、石棉网、酒精灯外还缺少的玻璃仪器是________
(2)写出焙烧时二氧化锗与氢氧化钠发生反应的化学方程式________________________________
(3)“酸化”至溶液中盐酸浓度为5.3 mol/L时有利于生成GeCl4,写出该反应的化学方程式:____若滤液“酸化”时酸度不够,溶液会出现明显的浑浊,原因是____________
(4)GeO2产品中通常混有少量SiO2。取样品w g,测得其中氧原子的物质的量为n mol,则该样品中GeO2的物质的量为____________mol(用含w、n的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】计算填空
(1)标准状况下,密度为0.75g·L-1的NH3与CH4组成的混合气体中,NH3的体积分数为__________,该混合气体对氢气的相对密度为_________。
(2)19g某二价金属氯化物(ACl2)中含有0.4molCl-,则ACl2的摩尔质量是___;A的相对原子质量是______;ACl2的化学式是_________。
(3)已知agA和bgB恰好完全反应生成0.2molC和dgD,则C的摩尔质量为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com