
| A. | 18O2和16O2是两种不同的原子 | B. | 甲醇(CH3OH)属于离子化合物 | ||
| C. | N5和N2是氮元素的两种同位素 | D. | 由N5变成N2是化学变化 |
分析 A.18O2和16O2是单质;
B.依据甲醇分子结构中形成的化学键分析判断;
C.质子数相同中子数不同的原子互称同位素;
D.物理变化和化学变化的根本区别在于是否有新物质生成.如果有新物质生成,则属于化学变化;反之,则是物理变化.
解答 解:A.18O2和16O2是氧元素的两种单质,不是原子,故A错误;
B.甲醇(CH3OH)是碳原子核氢原子氧原子间以共价键形成的共价化合物,属于有机共价化合物,故B错误;
C.N5和N2是单质,不是原子,故C错误;
D.2N5=5N2,有新的物质生成,属于化学变化,故D正确.
故选D.
点评 本题考查了核素、同素异形体的应用等,难度不大,关键是化合物的分类,同素异形体的转化是化学变化.


科目:高中化学 来源: 题型:选择题
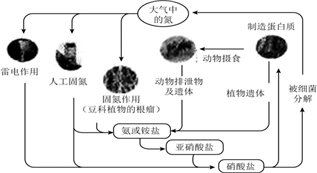
| A. | 氮元素均被氧化 | |
| B. | 工业合成氨属于人工固氮 | |
| C. | 含氮无机物和含氮有机物可相互转化 | |
| D. | 碳、氢、氧三种元素也参加了氮循环 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(OH-)=c(Na+)+c(H+) | |
| B. | 该溶液中的c(OH-)=1.0×10-3mol•L-1 | |
| C. | 加水稀释104倍所得溶液显碱性 | |
| D. | 与pH=3的HF溶液等体积混合所得溶液:c(Na+)=c(F-)+c(HF) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
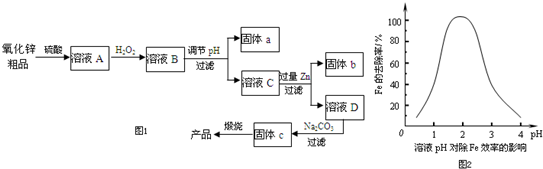
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在醋酸溶液中,NH4+、Na+、SiO32-、C2O42-能大量共存 | |
| B. | 与Na2S2O3溶液反应的离子方程式:S2O32-+2H+═S↓+SO2↑+H2O | |
| C. | 常温下,加水稀释醋酸,$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$增大 | |
| D. | 该醋酸溶液中c(CH3COO-)<0.001 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

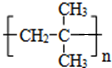 .
.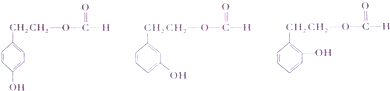 .
. $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +H2O.
+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com