
分析 n(H2SO4)=0.5L×0.2mol/L=0.1mol,n(KOH)=$\frac{11.2g}{56g/mol}$=0.2mol,则生成0.2molH2O(l)放出热量11.46kJ,生成1molH2O(l)放出热量为$\frac{11.46kJ}{0.2}$=57.3kJ,以此来解答.
解答 解:n(H2SO4)=0.5L×0.2mol/L=0.1mol,n(KOH)=$\frac{11.2g}{56g/mol}$=0.2mol,则生成0.2molH2O(l)放出热量11.46kJ,生成1molH2O(l)放出热量为$\frac{11.46kJ}{0.2}$=57.3kJ,则表示该反应中和热的化学方程式为为$\frac{1}{2}$H2SO4(aq)+KOH(aq)=$\frac{1}{2}$K2SO4(aq)+H2O(l)△H=-57.3kJ•mol-1,
故答案为:$\frac{1}{2}$H2SO4(aq)+KOH(aq)=$\frac{1}{2}$K2SO4(aq)+H2O(l)△H=-57.3kJ•mol-1.
点评 本题考查热化学方程式的书写,为高频考点,把握反应中能量变化、物质的量与热量的关系为解答的关键,侧重分析与应用能力的考查,注意中和热的判断,题目难度不大.


科目:高中化学 来源: 题型:填空题
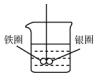 如图所示的装置,在盛有水的烧杯中,铁圈和银圈的连接处吊着一根绝缘的细丝,使之平痕.小心地从烧杯中央滴入CuSO4溶液.
如图所示的装置,在盛有水的烧杯中,铁圈和银圈的连接处吊着一根绝缘的细丝,使之平痕.小心地从烧杯中央滴入CuSO4溶液.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热 | B. | 不能稀硫酸而用浓硫酸 | ||
| C. | 往溶液中加入少量CuSO4固体 | D. | 不能铁片而用铁粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Na和O2 | B. | NaOH和SO2 | C. | NaHCO3和NaOH | D. | Na2CO3和HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 2 mol•L-1NaCl溶液中含有Na+个数为2NA | |
| B. | 标准态况下,22.4 LH2O含有水分子数为NA | |
| C. | 71g氯气与足量铁粉充分反应,转移的电子数为3NA | |
| D. | 标准状况下,16gO2和O3的混合气体中原子的物质的量为1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物理过程,吸收热量 | B. | 化学过程,吸收热量 | ||
| C. | 物理过程,放出热量 | D. | 化学过程,放出热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
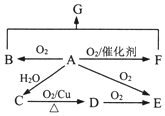 已知A石油裂解的主要产物,相对分子质量为28.B为气体,在标准状况下的密度为1.96g/L.D与F互为同分异构体,F是环状化合物.G的结构简式为:
已知A石油裂解的主要产物,相对分子质量为28.B为气体,在标准状况下的密度为1.96g/L.D与F互为同分异构体,F是环状化合物.G的结构简式为: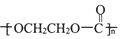 ,在一定条件下,它们有如图转化关系.
,在一定条件下,它们有如图转化关系.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com