
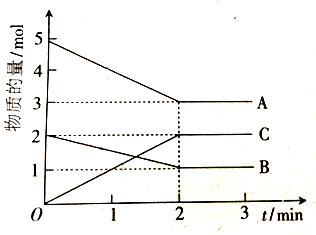
分析 (1)根据在反应中减小的物质为反应物,增加的物质为生成物,各物质的物质的量的变化量之比等于反应中各物质的计量数之比,写出化学方程式;
(2)由反应方程式为:2A+B?2C,一段时间后,C的浓度增加了3.0 mol•L-1,则B的浓度减少了$\frac{3.0mol/L}{2}$=1.5mol/L,根据时间△t=$\frac{△c}{v}$计算.
解答 解:(1)由图可知,在2min时,A的物质的量减小5mol-3mol=2mol,A为反应物,B的物质的量也减小2mol-1mol=1mol,B也为反应物,C的物质的量增加2mol,则C为生成物,A、B、C的物质的量的变化量之比为2:1:2,根据反应中的计量数之比等于变化的物质的物质的量之比,又因为2min时A、B都有剩余,所以为可逆反应,则反应方程式为:2A+B?2C,故答案为:2A+B?2C;
(2)由反应方程式为:2A+B?2C,一段时间后,C的浓度增加了3.0 mol•L-1,则B的浓度减少了$\frac{3.0mol/L}{2}$=1.5mol/L,又B表示的反应速率为1.0 mol•L-1•min-1,所以时间△t=$\frac{△c}{v}$=$\frac{1.5mol/L}{1.0mol/(L•min)}$=1.5min,
故答案为:1.5min.
点评 本题主要考查了根据图象写化学方程式、计算反应时间,内容比较简单,注重对基础知识的考查.


科目:高中化学 来源: 题型:选择题
| A. | 回收废旧电池 | |
| B. | 将工厂烟囱加高,减少周围大气污染 | |
| C. | 开发利用氢能源 | |
| D. | 推广使用无磷洗涤剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
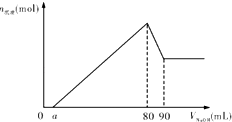 将一块镁铝的合金投入1mo1•L-1的一定体积的稀盐酸中,待合金完全溶解后,往溶液里滴入1mo1•L-1的NaOH溶液,生成沉淀物质的量与加入NaOH溶液体积(单位mL)的关系如图.下列说法中不正确的是( )
将一块镁铝的合金投入1mo1•L-1的一定体积的稀盐酸中,待合金完全溶解后,往溶液里滴入1mo1•L-1的NaOH溶液,生成沉淀物质的量与加入NaOH溶液体积(单位mL)的关系如图.下列说法中不正确的是( )| A. | 由图可以确定该镁铝合金中铝的质量为0.27g | |
| B. | 当滴入1mo1•L-1的NaOH溶液85mL时,所得沉淀为Mg(OH)2和Al(OH)3 | |
| C. | 由图可以确定a的取值范围为:0≤a≤50 | |
| D. | 由图可以确定该合金中镁铝物质的量之比0<$\frac{n(Mg)}{n(AI)}$<2.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③ | C. | ①⑤⑥ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应后的溶液的质量相同 | B. | 与浓硝酸的反应中,铜片先消失 | ||
| C. | 产生气体的颜色相同 | D. | 产生气体的体积相同(相同条件) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
(1)有机物X 的质谱图为: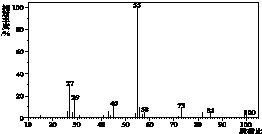 | (1)有机物X的相对分子质量是100. |
| (2)将10.0g X在足量O2中充分燃烧,并使其产物依次通过足量的无水CaCl2和KOH浓溶液,发现无水CaCl2增重7.2g,KOH浓溶液增重22.0g. | (2)有机物X的分子式是 C5H8O2. |
| (3)经红外光谱测定,有机物X中含有醛基;有机物X的核磁共振氢谱图上有2个吸收峰,峰面积之比是3:1. | (3)有机物X的结构简式是 (CH3)2C(CHO)2. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
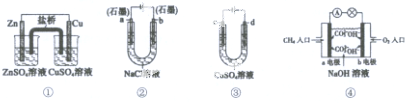
| A. | 装置①中,盐桥中的K+移向ZnSO4溶液 | |
| B. | 装置②工作一段时间后,a极附近溶液的pH增大 | |
| C. | 用装置③精炼铜时,c极为粗铜 | |
| D. | 装置④电池负极的电极反应式为:O2+4e-+2H2O=4OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com