
【题目】如下图,a、b是石墨电极,通电一段时间后,b极附近溶液显红色。下列说法正确的是
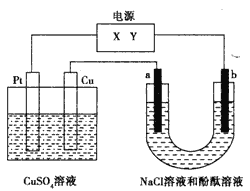
A. Pt为阴极,Cu为阳极
B. b极的电极反应式是2H++2e-=H2↑
C. 电解过程中CuSO4溶液的pH逐渐增大
D. Pt极上有6.4 g Cu析出时,b极产生2.24 L(标准状况)气体
科目:高中化学 来源: 题型:
【题目】研究证明高铁酸钠(Na2FeO4) 是一种“绿色环保高效”消毒剂, 比目前国内外广泛使用的含氯饮用水消毒剂性能更为优良。高铁酸钠只能在碱性环境中稳定存在。下列是通过次氯酸钠氧化法制备高铁酸钠并探究其性质的实验,步骤如下:
I.用氯气和氢氧化钠溶液反应制备NaClO溶液
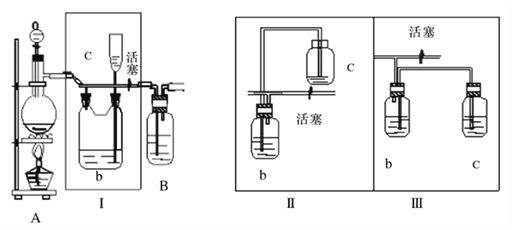
(1)A是氯气发生装置,写出实验室用此装置制取氯气的离子方程式__________。
(2)I装置的作用是__________ 。
(3)用图示的II或III代替I是否可行? __________。简要说明理由__________ 。
(4)将产生的氯气通入D装置中制NaClO溶液
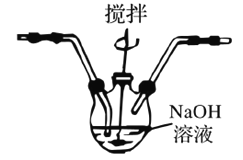
已知:3Cl2+6NaOH![]() 5NaCl+NaClO3+3H2O 为了防止产生NaClO3,除搅拌和混入N2稀释外,还应采取的操作是__________。
5NaCl+NaClO3+3H2O 为了防止产生NaClO3,除搅拌和混入N2稀释外,还应采取的操作是__________。
II.制备Na2FeO4
(1)将Fe(NO3)3溶液加入到NaOH与NaClO的混合溶液中,其反应的离子方程式是______。过滤得到粗产品,再用NaOH溶液溶解,重结晶,用有机溶剂脱碱,低温烘干得到固体样品,上述制备过程中,用NaOH溶液溶解粗产品而不用水的原因是__________。
(2)高铁酸钠电池是一种新型可充电电池,电解质为NaOH溶液,放电时负极材料为Zn,正极产生红褐色沉淀,写出该电池反应的化学方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋是资源宝库。下图是工业上对海水的一种综合利用的流程图:

请回答下列问题:
(1) 在实验室对海水进行过滤,所需要玻璃仪器为烧杯、漏斗和_________。
(2) 若粗盐中含有Ca2+、Mg2+、SO42-三种杂质离子。精制提纯时,备用的除杂试剂有:A.盐酸,B.Na2CO3溶液,C.NaOH溶液,D.BaCl2溶液。请你正确排列加入试剂的顺序:NaOH溶液、_______、_______、_______(填编号)。
(3) 用如图电解食盐水,石墨电极上产生的气体为_______;在铁棒周围的溶液里滴加酚酞试剂,溶液变_______色;小烧杯中NaOH溶液的作用是(用化学方程式表示):______________。

(4)在盛有Mg(OH)2固体的烧杯中,加入足量盐酸,待固体全部溶解后,要从溶液中获取MgCl2·6H2O晶体,需要进行的实验操作依次为_________________(填编号)。
A.蒸馏 B.蒸发 C.冷却结晶 D.过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z、R 原子序数依次增大。由W、X、Y、R组成的一种化合物a在加热时完全分解为三种产物,其中一种产物b是能使品红溶液褪色的气体,另一种产物c是能使湿润的红色石蕊试纸变蓝的气体。金属单质Z在空气中燃烧生成的化合物可与水发生反应生成气体。下列说法正确的是
A. 简单离子的半径: X < Z < R
B. X的简单氢化物比Y的稳定
C. a、b、c中均含有极性共价健,且 a属于电解质,b和c都属于非电解质
D. W、X、Y、R四种元素形成的化合物一定会促进水的电离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用元素的化合价推测物质的性质是化学研究的重要手段.如图是硫元素的常见化合价与部分物质类别的对应关系:
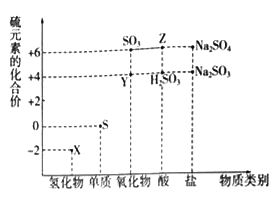
(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有_______(填化学式).
(2)将X与Y混合,可生成淡黄色固体.该反应中氧化剂与还原剂的物质的量之比为_______.
(3)检验物质Y的方法是_______________________________.
(4)Z的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为_______.
(5)Na2S2O3是重要的化工原料.从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是______(填代号).
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(6)已知Na2SO3能被K2Cr207氧化为Na2SO4则24mL 0.05molL﹣1的Na2SO3溶液与 20mL 0.02molL﹣1的溶液恰好反应时,Cr元素在还原产物中的化合价为________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、目前世界上60%的镁是从海水中提取的。海水提镁的主要流程如下:
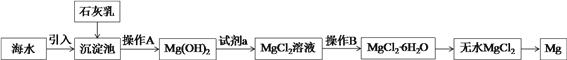
操作A是____________,下列仪器中操作B必须使用的有__________(填字母符号)。
A、锥形瓶 B、玻璃棒 C、表面皿 D、蒸发皿 E、坩埚
Ⅱ、乙醇镁[(CH3CH2O)2Mg] 为白色固体,难溶于乙醚和烃类,略溶于乙醇,在空气中会水解,常用作烯烃聚合催化剂载体和制备精密陶瓷的原料。某小组同学用镁粉(受潮会发生自燃、自爆)与乙醇在实验室中制备乙醇镁:
(1)干燥管中盛装的试剂为_____________,其作用为__________________________。
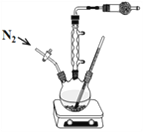
(2)下列操作的合理顺序为:______________。
a、将干燥的氮气通入装置,连续操作数次;
b、称取镁粉,量取无水乙醇加入反应器内;
c、加热回流,控制温度在80℃,反应1小时;
d、开启冷凝水和磁力搅拌器。
(3)将温度控制在80℃的原因是________________,写出生成乙醇镁的化学方程式____________________________。
(4)请你设计实验证明有乙醇镁生成(简述实验的方法):_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:①Cl2+2KBr=2KCl+Br2, ②KClO3+6HCl=3Cl2+KCl +3H2O,
③2KBrO3+Cl2=Br2+ 2KClO3,下列说法正确的是
A. 上述三个反应都有单质生成,所以都是置换反应
B. 氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2
C. 反应②中还原剂与氧化剂的物质的量之比为6:1
D. ③中lmol还原剂反应则氧化剂得到电子的物质的量为2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置能达到实验目的的是
A. 碳酸氢钠溶液直接蒸干得到碳酸氢钠固体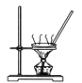
B. 制备Fe(OH)2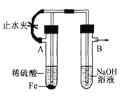
C. 除去CO2中含有的少量HCl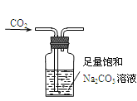
D. 配制100mL 0.1mol/L的稀硫酸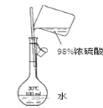
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]() 、
、![]()
I.冠心平F是降血脂、降胆固醇的药物,它的一条合成路线如下:
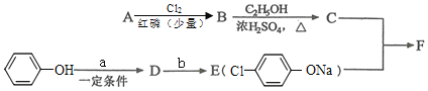
(1)A为一元羧酸,8.8gA与足量NaHCO3溶液反应生成2.24LCO2(标准状况),A的分子式为____________。
(2)写出符合A分子式的所有甲酸酯的结构简式:________________。
(3)B是氯代羧酸,其核磁共振氢谱有两个峰,写出B→C的反应方程式:____________。
(4)C+E→F的反应类型为____________。
(5)写出A和F的结构简式:____________。
(6)D的苯环上有两种氢,它所含官能团的名称为_____________;写出b所代表的试剂为____________。
II.有机物H的分子式为C2H2O3,可发生银镜反应,且具有酸性。
(7)H有多种合成方法,在方框中写出由乙酸合成H的路线流程图(其他原料任选)。合成路线流程图示例如下:![]() ________________________________________________。
________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com