
A~F六种有机物的相互转化关系如图所示:

已知:

据此回答下列问题:
(1)A是合成天然橡胶的单体,用系统命名法命名,A的名称为 ,天然橡胶的结构简式为 。
(2)A生成 时,A发生的反应类型为
。
时,A发生的反应类型为
。
(3) E→F的化学方程式为 。
(4)A与Br2按物质的量比1:1发生加成反应,生成的产物有____种(考虑顺反异构)。
(5)现有另一种有机物G,已知G与E无论按何种比例混合,只要总质量一定,完全燃烧时生成的CO2、H2O以及消耗的O2均为定值。请写出两种符合下列要求的G的结构简式____、 。
① ;
;
②G的核磁共振氢谱表明其有两种不同化学环境的氢,且峰面积比为1:3。
(1)2-甲基-1,3-丁二烯;
(2)1,4-加成反应
(3)
或 
(4)4
(5)CH3COOH;HCOOCH3
【解析】
试题解析:根据已知信息①,可知A中含有两个碳碳双键,结合已知信息②,A被氧化后只有两种产物,则可判断A的结构为CH2=C(CH3)CH=CH2;根据C生成的D可与H2发生反应,可判断D中除羧基外还有醛基,因此根据信息②,B为HCHO,C为 ,C中醛基被氧化生成的D为
,C中醛基被氧化生成的D为 ,D加氢得到的E为CH3CH(OH)COOH,E中的羧基和羟基缩聚得到的F为
,D加氢得到的E为CH3CH(OH)COOH,E中的羧基和羟基缩聚得到的F为 。
。
(1)根据系统命名法,A的名称为2-甲基-1,3-丁二烯;天然橡胶是A发生1,4加聚得到的高聚物,因此天然橡胶的结构简式为 。
。
(2)根据已知信息①,可知A发生1,4-加成反应。
(3)E→F是羧基和羟基发生缩聚反应。
(4)A与Br2按物质的量比1:1发生加成的产物有CH2BrCBr(CH3)CH=CH2、CH2=C(CH3)CHBrCH2Br、CH2BrC(CH3)=CHCH2Br,第三种产物有顺反异构体,因此共有4种。
(5)G与E无论按何种比例混合,只要总质量一定,完全燃烧时生成的CO2、H2O以及消耗的O2均为定值,则可知G与E中C、H、O的个数比相同,结合题中要求,可知G的分子式为C2H4O2,因此其同分异构体有CH3COOH;HCOOCH3两种。
考点:考查有机物的结构简式,官能团的性质,有机反应类型,有机物命名,同分异构体判断与书写,有机反应方程式书写。


科目:高中化学 来源: 题型:
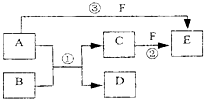 A、B、C、D、E、F六种物质的相互转化关系如下图所示(反应条件未标出),
A、B、C、D、E、F六种物质的相互转化关系如下图所示(反应条件未标出),
| ||
| △ |
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (2011?山西模拟)A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件未标出),其中反应①是置换反应.
(2011?山西模拟)A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件未标出),其中反应①是置换反应.
| ||
| ||


| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
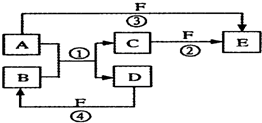 (2010?海南模拟)A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件未标出),其中反应①是置换反应,A是常见的金属单质,D是无色气体单质、F是黄绿色气态单质,反应①②均在水溶液中进行的.
(2010?海南模拟)A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件未标出),其中反应①是置换反应,A是常见的金属单质,D是无色气体单质、F是黄绿色气态单质,反应①②均在水溶液中进行的.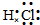
| 2a |
| 3 |
| 2a |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F六种物质的相互转化关系如下图所示(反应条件及部分产物未标出)。

(1)若A、D、F都是非金属单质,常温下,A、D为固体,D单质可作为半导体材料,F为气体,且A、D所含元素为同主族短周期元素,A、F所含元素同周期,则反应①的化学方程式是___________________________。
(2)若A是常见的金属单质,D、F是气态单质,反应①在水溶液中进行,C的溶液为浅绿色,则反应②(在水溶液中进行)的离子方程式是:_____________________________;已知1gD与足量F在光照的条件下完全反应生成B时,放出92.3 kJ热量,试写出该反应的热化学方程式:_______________。工业上可用电解方法同时制得D和F,写出电解过程中阳极的电极反应式:________________________________________.
(3)若B、C、F都是气态单质,且B有毒呈黄绿色,反应③中有水生成,反应②需要放电才能发生,A、D相遇有白烟生成,则反应③的化学方程式是_________________。
(4)若A、B、D为有机物,B的相对分子质量比A大14,E、F为无机物单质,C为最常见的氧化物,通常状况下为液态,C能与乙烯在一定条件下发生加成反应生成A。则E的化学式为_______________,D的结构简式为______________,反应①属于__________反应,反应③的化学方程式为_______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com