
将4.0 mol PCl3和2.0 mol Cl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g)PCl5(g)。达到平衡时,PCl5为0.80 mol,如果此时移走2.0 mol PCl3和1.0 mol Cl2,在相同温度下再达平衡时PCl5的物质的量是( )
A.0.8 mol B.0.4 mol
C.小于0.4 mol D.大于0.4 mol,小于0.8 mol
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
某合作小组同学将铜片加入稀硝酸中,发现开始时反应非常慢,一段时间后反应速率明显加快。该小组通过实验探究其原因。
(1)该反应的离子方程式为______________________________________。
(2)提出合理假设,该实验中反应速率明显加快的原因可能是______(填字母)。
A.反应放热导致温度升高
B.压强增大
C.生成物的催化作用
D.反应物接触面积增大
(3)初步探究,测定反应过程中不同时间溶液的温度,结果如表所示:
| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 35 | 50 | 60 | 70 | 80 |
| 温度/℃ | 25 | 26 | 26 | 26 | 26 | 26 | 26.5 | 27 | 27 | 27 | 27 |
结合实验目的和表中数据,你得出的结论是__________________________。
(4)进一步探究:查阅文献了解到化学反应的产物(含中间产物)可能对反应有催化作用。请完成以下实验设计表并将实验目的补充完整:
| 实验编号 | 铜片质量/g | 0.1 mol·L-1的硝酸体积/mL | 硝酸铜晶体/g | 亚硝酸钠晶体/g | 实验目的 |
| ① | 5 | 20 | 实验①和②探究____的影响;实验①和③探究NO | ||
| ② | 0.5 | ||||
| ③ | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
①有化学键破坏的变化一定属于化学变化 ②发生颜色变化的一定是化学变化 ③电解的过程一定发生化学变化 ④用糯米、酒曲和水制成甜酒酿,一定是化学变化
A.①③ B.②③④ C.③④ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法:

①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是_________________________________________________________________
(用离子方程式表示)。为将碱洗槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的________。
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为________。取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,产生沉淀的原因是______________________________________________
_______________________________________________________________。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是_______________________________________________________________。
(3)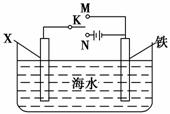 利用右图装置,可以模拟铁的电化学防护。
利用右图装置,可以模拟铁的电化学防护。
若X为碳棒,为减缓铁的腐蚀,开关K应置于________处。若X为锌,开关K置于M处,该电化学防护法称为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对于以下三个反应,从正反开始进行达到平衡后,保持温度、体积不变,按要求回答下列问题。
(1)PCl5(g)PCl3(g)+Cl2(g)
再充入PCl5(g)平衡向________方向移动,达到平衡后,PCl5(g)的转化率________,PCl5(g)的百分含量______。
(2)2HI(g)I2(g)+H2(g)
再充入HI(g)平衡向________方向移动,达到平衡后,HI的分解率________,HI的百分含量________。
(3)2NO2(g)N2O4(g)
再充入NO2(g),平衡向________方向移动,达到平衡后,NO2(g)的转化率________,NO2(g)的百分含量________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应CO(g)+H2O(g)CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下( )
A.加入催化剂,改变了反应的途径,反应的ΔH也随之改变
B.改变压强,平衡不发生移动,反应放出的热量不变
C.升高温度,反应速率加快,反应放出的热量不变
D.若在原电池中进行,反应放出的热量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
在容积为2 L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,考察温度对反应的影响 ,实验结果如下图所示(注:T1、T2均大于300 ℃):
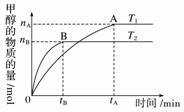
下列说法正确的是____(填序号)。
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为
v(CH3OH)=mol·L-1·min-1
②该反应在T1时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时增大
(4)在T1温度时,将1 mol CO2和3 mol H2充入一密闭恒容容器中,充分反应达到平衡后,若CO2的转化率为α,则容器内的压强与起始压强之比为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
在100℃时,将N2O4、NO2分别充入两个各为1 L的密闭容器中,反应过程中浓度变化如下:[2NO2(g)  N2O4(g) ΔH<0]
N2O4(g) ΔH<0]
| 容器 | 物质 | 起始浓度/(mol·L-1) | 平衡浓度/(mol·L-1) |
| Ⅰ | N2O4 | 0.100 | 0.040 |
| NO2 | 0 | 0.120 | |
| Ⅱ | N2O4 | 0 | 0.014 |
| NO2 | 0.100 | 0.072 |
下列说法正确的是
A. 平衡时,Ⅰ、Ⅱ中反应物的转化率α(N2O4)<α(NO2)
B. 平衡时,Ⅰ、Ⅱ中上述正反应的平衡常数K(Ⅰ) = 2K(Ⅱ)
C. 平衡后,升高相同温度,以N2O4表示的反应速率ν(Ⅰ)<ν(Ⅱ)
D. 平衡后,升高温度,Ⅰ、Ⅱ中气体颜色都将变深
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com