
常温下,有下列4种溶液,下列说法正确的是 ( )
| ① | ② | ③ | ④ |
| 0.1 mol·L-1 CH3COOH溶液 | pH=3 CH3COOH溶液 | 0.1 mol ·L-1 NaOH溶液 | pH=11 NaOH溶液 |
A.由水电离出的c(H+):③>①
B.①稀释到原来的100倍后,pH与②相同
C.①与③混合,若溶液pH=7,则两种溶液的体积:③>①
D.②与④混合,若溶液pH=7,则两种溶液的体积:④>②
科目:高中化学 来源: 题型:
下列实验“操作和现象”与“结论”对应关系正确的是
| 选项 | 实验操作及现象 | 实验结论 |
| A | 用铂丝做某溶液的焰色反应,火焰呈黄色 | 该溶液中一定含有钠盐 |
| B | 将二氧化硫通入到溴水中,溴水褪色 | 二氧化硫具有漂白性 |
| C | 在滴有酚酞的Na2CO3溶液中,滴加入BaC12溶液,溶液红色逐渐褪去。 | Na2CO3溶液中存在水解平衡 |
| D | 某钾盐溶于盐酸,产生能使澄清石灰水变浑浊的无色无味气体 | 该钾盐是K2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应:AgF+Cl2+H2O→AgCl+AgClO3+HF+O2(未配平),下列说法不正确的是
A.AgClO3是氧化产物
B.方程式的计量数依次为:10,5,5,9,1,10,1
C.反应转移4mole-时生成标准状况下22.4 L O2
D.被还原的氯原子与被氧化的氯原子质量比为9︰1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A.在一定温度下的AgCl水溶液中,Ag+和Cl-浓度的乘积是一个常数
B.AgCl的Ksp=1.8×10-10 mol2·L-2,在任何含AgCl固体的溶液中,[Ag+]=[Cl-],且Ag+和Cl-浓度的乘积等于1.8×10-10mol2·L-2
C.温度一定时,在AgCl饱和溶液中,Ag+和Cl-浓度的乘积是一个常数
D.向饱和AgCl溶液中加入盐酸,Ksp变大
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,0.1mol·L—1某一元酸(HA)溶液中c(OH—)/c(H+)=1×10—8,下列叙述正确的是
A.溶液中水电离出的c(H+)=10—10mol·L—1
B.溶液中c(H+)+c(A—)=0.1mol·L—1
C.与0.05mol·L—1 NaOH溶液等体积混合所得溶液中离子浓度大小关系为:
c(A—)> c(Na+)> c(OH—)> c(H+)
D.原溶液中加入一定量CH3COONa晶体或加水稀释,溶液的c(OH—)均增大
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25 ℃时部分弱电解质的电离平衡常数数据如下表:
| 弱酸化学式 | HSCN | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.3×10-1 | 1.7×10-5 | 6.2×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
回答下列问题:
(1)写出碳酸的第一级电离平衡常数表达式:K1=_______________________。
(2)等物质的量浓度的a.CH3COONa、b.NaCN、c.Na2CO3、d.NaHCO3溶液的pH由大到小的顺序为 ___ _____(填字母)。
(3) 常温下,0.1 mol·L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是 (填序号)
A.[H+] B.[H+]/[CH3COOH] C.[H+]·[OH-] D.[OH-]/[H+]
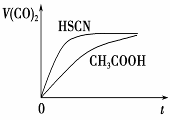 (4)25 ℃时,将20 mL 0.1 mol·L-1 CH3COOH溶液和20mL0.1 mol·L-1HSCN溶液分别与20 mL 0.1 mol·L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如右图所示:反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是
(4)25 ℃时,将20 mL 0.1 mol·L-1 CH3COOH溶液和20mL0.1 mol·L-1HSCN溶液分别与20 mL 0.1 mol·L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如右图所示:反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是
反应结束后所得两溶液中,c(CH3COO-)________c(SCN-)(填“>”、“<”或“=”)
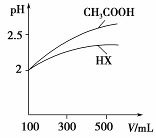 (5)体积均为100 mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如右图所示,则HX的电离平衡常数________(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数。
(5)体积均为100 mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如右图所示,则HX的电离平衡常数________(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数。
(6)25 ℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=________mol·L-1(填精确值),
c(CH3COO-)/c(CH3COOH)=________。
(7) 写出少量CO2通入次氯酸钠溶液中的离子方程式:
______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下列反应的热化学方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l) △H1
2 H2(g)+ O2(g)= 2H2O(g) △H2
C(s)+ O2(g)=CO2(g) △H3
则反应4C3H5(ONO2)3(l)= 12CO2(g)+10H2O(g) + O2(g) +6N2(g)的△H为
A.12△H3+5△H2-2△H1 B.2△H1-5△H2-12△H3
C.12△H3-5△H2-2H1 D.△H1-5△H2-12△H3
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度条件下,甲、乙两个容积相等的恒容密闭容器中均发生如
下反应:3A(g)+B(g)  xC(g)+D(s),向甲中通入6molA和2 molB,向乙中通入1.5molA、0.5molB、3molC和2molD,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为20%,下列叙述中不正确的是
xC(g)+D(s),向甲中通入6molA和2 molB,向乙中通入1.5molA、0.5molB、3molC和2molD,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为20%,下列叙述中不正确的是
A.若平衡时,甲、乙两容器中A的物质的量不相等,则x=4
B.平衡时,甲、乙两容器中A、B的物质的量之比相等
C.平衡时甲中A的体积分数为40%
D.若平衡时两容器中的压强不相等,则两容器中压强之比为8:5
查看答案和解析>>
科目:高中化学 来源: 题型:
利用碳酸钠晶体(Na2CO3·10H2O)来配制0.1 mol·L-1的Na2CO3溶液500 mL。
(1)应称取碳酸钠晶体________g。
(2)若称量时砝码与晶体位置左右颠倒,则平衡后实际称得的样品质量为________g(5 g以下使用游码)。
(3)配制溶液时需要用到的仪器有____________________________________。
(4)假如其他操作均准确无误,下列情况会引起所配溶液浓度偏高的是________。
A.容量瓶洗净后内壁上带有少量蒸馏水
B.定容时,俯视观察刻度线
C.移液时,用于溶解碳酸钠晶体的烧杯没有冲洗
D.定容后,将容量瓶振荡摇匀,静置时发现液面低于刻度线,于是又加入少量水至刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com