
 ,它在一定条件下可能发生的反应有( )
,它在一定条件下可能发生的反应有( )| A. | ①③④ | B. | ①③④⑤ | C. | ②③④ | D. | ①③⑤ |
分析 该物质中含有醇羟基、苯环、羧基和醛基,具有醇、苯、羧酸和醛的性质,能发生酯化反应、取代反应、氧化反应、加成反应、缩聚反应、银镜反应等,据此分析解答.
解答 解:该物质中含有醇羟基、苯环、羧基和醛基,具有醇、苯、羧酸和醛的性质,
苯环和醛基能发生加成反应;
不含酯基或卤原子,则不能发生缩聚反应;
羧基和醇羟基能发生酯化反应;
醇羟基、醛基能发生氧化反应;
连接醇羟基碳原子相邻碳原子上不含氢原子,则不能发生消去反应,
故选A.
点评 本题考查有机物结构和性质,为高频考点,侧重考查学生分析判断能力,明确官能团及其性质关系是解本题关键,侧重考查醇、醛、羧酸和苯环性质,注意能发生消去反应的醇结构特点,题目难度不大.


科目:高中化学 来源: 题型:解答题
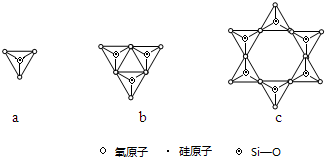
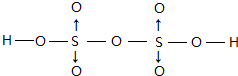 (配位键须注明).
(配位键须注明).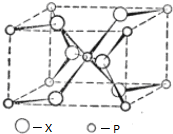
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯分子中的所有原子可能共平面 | B. |  分子中的所有原子可能共平面 分子中的所有原子可能共平面 | ||
| C. | 乙烷分子中的所有原子可能共平面 | D. | 二氯甲烷分子为正四面体结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 如图是研究部分元素氢化物的沸点变化规律的图象,折线c可以表达出第ⅣA族元素氢化物的沸点变化规律.两位同学对某主族元素氢化物的沸点的变化趋势画出了两条折线--折线a和折线b,你认为正确的是b(填“a”或“b”),理由是A点所示的氢化物是水,其沸点高是由于水分子间存在氢键,所以氧族元素中其他氢化物的沸点不会高于水.
如图是研究部分元素氢化物的沸点变化规律的图象,折线c可以表达出第ⅣA族元素氢化物的沸点变化规律.两位同学对某主族元素氢化物的沸点的变化趋势画出了两条折线--折线a和折线b,你认为正确的是b(填“a”或“b”),理由是A点所示的氢化物是水,其沸点高是由于水分子间存在氢键,所以氧族元素中其他氢化物的沸点不会高于水.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 金属镁及其化合物在生活、工农业生产等方面有广泛的应用.
金属镁及其化合物在生活、工农业生产等方面有广泛的应用.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,
, ,稳定性较好.
,稳定性较好.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com