
| A、乙酸能发生酯化反应,而碳酸不能 |
| B、碳酸和乙酸都能与碱反应,产物都是弱碱性的盐 |
| C、乙酸易溶于水,在水中的溶解度较大,而碳酸的溶解度较小 |
| D、醋酸可用于清除水垢 |


科目:高中化学 来源: 题型:
A、 构成锌铜原电池 |
B、 测定酸碱中和反应中和热大小的量热计 |
C、 验证CaO和水反应的热效应 |
D、 证明电解食盐水时阳极有Cl2,阴极有NaOH生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用托盘天平称取NaCl固体23.4g |
| B、应选用500mL的容量瓶来配制此溶液 |
| C、在转移操作中不慎将溶液洒到容量瓶外面,应该重新配置溶液 |
| D、加蒸馏水至离刻度线1-2cm时改用胶头滴管定容 |
查看答案和解析>>
科目:高中化学 来源: 题型:
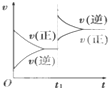 对达到平衡状态的可逆反应:A+B?C+D,在t1时增大压强,则正、逆反应速率变化如图所示(v表示反应速率,t代表时间),下列有关A、B、C、D的状态叙述正确的是( )
对达到平衡状态的可逆反应:A+B?C+D,在t1时增大压强,则正、逆反应速率变化如图所示(v表示反应速率,t代表时间),下列有关A、B、C、D的状态叙述正确的是( )| A、A、B、C是气体,D不是气体 |
| B、A、B是气体,C、D有一种是气体 |
| C、C、D是气体,A、B有一种是气体 |
| D、A、B、C、D都是气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝箔在空气中受热熔化,并不滴落,说明铝与氧气没有发生化学反应 |
| B、NH3+H3O+═NH4++H2O说明结合H+的能力:H2O>NH3 |
| C、FeCl2、Fe(OH)3均可通过化合反应制得 |
| D、分子式为C2H4O2的化合物只能电离,不能水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、1:1 | B、1:2 |
| C、1:3 | D、1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
| 物质 | H2 | CO | CH3OH |
| 浓度/(mol?L-1) | 0.2 | 0.1 | 0.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 实验室需要0.80mol?L-1 NaOH溶液475mL和0.40mol?L-1硫酸500mL.根据这两种溶液的配制情况回答下列问题:
实验室需要0.80mol?L-1 NaOH溶液475mL和0.40mol?L-1硫酸500mL.根据这两种溶液的配制情况回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com