
已知N、P同属于元素周期表的第VA族元素,N在第2周期,P在第3周期。NH3
分子呈三角锥形,氮原子位于锥顶,三个氢原子位于锥底,N—H键间的夹角是107°。
(1)PH3分子与NH3分子的构型关系是________(填“相同”或“相似”或“不相似”),P—H______极
性(填“有”或“无”),PH3分子________极性(填“有”或“无”)。
(2)NH3与PH3相比,热稳定性________(填化学式)更强。
(3)NH3、PH3在常温、常压下都是气体,但NH3比PH3易液化,其主要原因是________.
A.键的极性N—H比P—H强 B.分子的极性NH3比PH3强
C.相对分子质量PH3比NH3大 D.NH3分子之间存在特殊的分子间作用力
(1)相似 有 有 (2)NH3 (3)D
【解析】
试题分析:(1)N和P都是第ⅤA族元素,其氢化物的结构是相似,所以pH3分子与NH3分子的构型关系是相似的。分子中的共价键均是极性键。
(2)氮元素的非金属性强于P元素的,则氨气的稳定性强于pH3的。
(3)由于氮元素是活泼的非金属元素,在氨气分子间存在氢键,所以氨气比pH3易液化,答案选D。
考点:考查元素周期律的应用、分子稳定性以及氢键的判断和应用
点评:该题主要是第ⅤA族中第N和P的氢化物为载体,重点考查学生运用物质结构理论解决实际问题的能力,有利于培养学生的逻辑推理能力和发散思维能力,有助于激发学生的学习兴趣和学习积极性。


科目:高中化学 来源: 题型:
已知:X为六元环状化合物
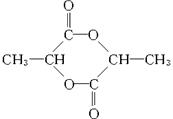
(1)A1的分子式为________________。
(2)写出下列物质的结构简式:A2____________,X____________。
(3)书写化学方程式:反应④____________;反应①属于____________反应,反应②属于____________反应。
(4)与G具有相同官能团的G的同分异构体M在酸性条件下,加热失水生成N,N的甲酯可以发生加聚反应生成聚合物P,写出M→N的化学方程式:____________。聚合物P的结构简式为________________________。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年吉林省汪清六中高二下学期期中考试化学试卷(带解析) 题型:填空题
已知N、P同属于元素周期表的第VA族元素,N在第2周期,P在第3周期。NH3
分子呈三角锥形,氮原子位于锥顶,三个氢原子位于锥底,N—H键间的夹角是107°。
(1)PH3分子与NH3分子的构型关系是________(填“相同”或“相似”或“不相似”),P—H______极
性(填“有”或“无”),PH3分子________极性(填“有”或“无”)。
(2)NH3与PH3相比,热稳定性________(填化学式)更强。
(3)NH3、PH3在常温、常压下都是气体,但NH3比PH3易液化,其主要原因是________.
| A.键的极性N—H比P—H强 | B.分子的极性NH3比PH3强 |
| C.相对分子质量PH3比NH3大 | D.NH3分子之间存在特殊的分子间作用力 |
查看答案和解析>>
科目:高中化学 来源:2012届山东省曲阜师大附中高三9月教学质量检测化学试卷 题型:填空题
(14分)有机物A1和A2含有碳、氢、氧三种元素且互为同分异构体。已知6 g A1在足量的氧气中完全燃烧生成13.2 g二氧化碳和7.2 g水。有关物质之间的转化关系如下: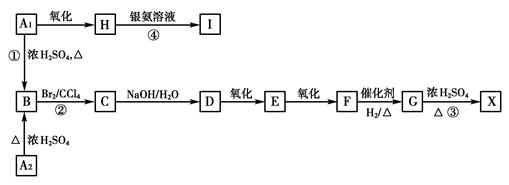
已知:X为六元环状化合物,完成下列问题:
(1)A1的分子式为_____________,X的结构简式:________________ 。
(2)E中含氧官能团的名称: 。
(3)反应④的化学方程式: ;
C到D 的化学方程式: ;
反应②属于__________ 反应。
(4)与G具有相同官能团的G的同分异构体M在酸性条件下,加热失水生成N,N的甲酯可以发生加聚反应生成聚合物P,聚合物P的结构为: 。
查看答案和解析>>
科目:高中化学 来源:2010年上海市虹口区高三第二次模拟考试化学试题 题型:填空题
组成生命细胞的11种宏量元素(约占人体总质量的99.97%),全部位于周期表的前20号。其中组成人体蛋白质、脂肪、碳水化合物和核酸的主要有6种元素。
(1)这六种元素中除H、C、O、P、S外,应该还有______(写元素符号),它的原子最外层共有______种不同运动状态的电子;与它同周期,且单质熔点最高的元素在周期表中的位置_______________________。
(2)糖类是人体获得能量的来源之一。已知1mol 葡萄糖在人体内完全氧化为二氧化碳和水,放出2804 kJ的热量,该反应的热化学方程式_______________________________________。
(3)CO2是一种温室气体,它的电子式为______________,将其转变其他化工原料,必须破坏的化学键属于_________(填“极性”或“非极性”)键。
(4)元素周期表中元素的性质存在递变规律,下列关系正确的是______(填序号)。
a.离子半径:S2—>Na+>O2—>H+ b.与水反应的剧烈程度:K>Na>Mg>Ca
c.熔点:CO2>SiO2>Na2O>SO3 d.还原性:PH3>H2S>HCl>HF
(5)下表为部分非金属元素与氢形成共价键的键长与键能数据:
|
共价键 |
H-H |
H-F |
H-Cl |
H-Br |
H-O |
H-S |
H-N |
H-P |
|
键长(pm) |
74 |
92 |
127 |
141 |
98 |
135 |
101 |
321 |
|
键能(kJ/mol) |
436 |
568 |
432 |
368 |
464 |
364 |
391 |
142 |
根据表中数据,归纳共价键键能与键长的关系_______________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com