
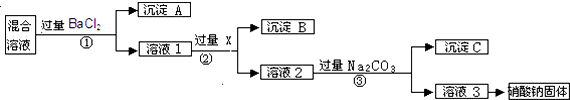
分析 由流程可知,①中加氯化钡,硫酸根离子转化为沉淀,则沉淀A为BaSO4,溶液1中含氯化钠、硝酸钠、氯化钡,②中加AgNO3后氯离子转化沉淀,沉淀B为AgCl,溶液2中含硝酸钠、硝酸银、硝酸钡,③中钡离子,银离子转化为沉淀,沉淀C为碳酸钡、碳酸银,溶液3为硝酸钠和碳酸钠,转化中试剂过量保证离子完全转化为沉淀,以此来解答.
解答 解:由流程可知,①中加氯化钡,硫酸根离子转化为沉淀,则沉淀A为BaSO4,溶液1中含氯化钠、硝酸钠、氯化钡,②中加AgNO3后氯离子转化沉淀,沉淀B为AgCl,溶液2中含硝酸钠、硝酸银、硝酸钡,③中钡离子,银离子转化为沉淀,沉淀C为碳酸钡、碳酸银,溶液3为硝酸钠和碳酸钠,
(1)由上述分析可知,X为AgNO3,沉淀A为BaSO4,故答案为:AgNO3;BaSO4;
(2)流程中①②③步均生成沉淀,需要进行过滤操作,故答案为:过滤;
(3)加入过量的Na2CO3的目的是使溶液中的Ag+、Ba2+完全沉淀,故答案为:使溶液中的Ag+、Ba2+完全沉淀;
(4)溶液3中肯定含有Na2CO3,可加适量的稀硝酸后蒸发结晶或加热冷却结晶得到纯净的硝酸钠,
故答案为:Na2CO3;稀HNO3;冷却热饱和溶液(或蒸发浓缩冷却结晶).
点评 本题考查物质分离、提纯实验方案的设计,为高考常见题型,侧重于学生的分析、实验能力的考查,把握流程中试剂的加入发生的化学反应及操作为解答的关键,注重实验的严密性和溶液的配制、物质提纯的考查,题目难度中等.


 星级口算天天练系列答案
星级口算天天练系列答案科目:高中化学 来源: 题型:解答题
 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜和稀硝酸的反应:Cu2++4H++2NO3-═Cu2++2NO2↑+2H2O | |
| B. | 氯气与水反应:Fe3++Cu═Fe2++Cu2+ | |
| C. | 氯化铝溶液加入氨水:Al3++3OH-═Al(OH)3↓ | |
| D. | 实验室制氯气:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定含有CO32- | B. | 一定含有Ag+ | ||
| C. | 一定含有SO42- | D. | 可能含有SO42-也可能含有Ag+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. 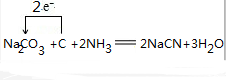 .
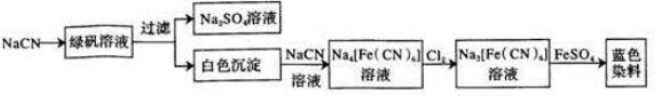
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 510 | 770 | 918 |
| 气体体积/mL | 560 | 672 | 672 |
| A. | 甲组和乙组的实验中,盐酸均是过量的 | |
| B. | 盐酸的物质的量浓度为1.0mol•L-1 | |
| C. | 合金中镁铝的物质的量之比为1:1 | |
| D. | 丙组中铝的物质的量为0.018mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com