
| A. | 同周期的主族元素从左到右原子半径逐渐减小,它们形成简单的离子半径逐渐增大 | |
| B. | 可以根据主族元素原子的电子层数和最外层电子数确定其在周期表中的位置 | |
| C. | 由氟、氯两元素在周期表中位置关系推知,氟元素非金属性强于氯元素,所以氢氟酸的酸性应强于盐酸 | |
| D. | 在实际生产中,多在元素周期表的过渡元素区寻找新型半导体材料 |
分析 A.同周期的主族元素从左向右原子半径减小,电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越大;
B.对于主族元素周期数=电子层数、主族族序数=最外层电子数;
C.HF属于弱酸,而HCl属于强酸;
D.在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素.
解答 解:A.同周期的主族元素从左向右核电荷数增大,则原子半径减小,阴离子比阳离子对1个电子层,简单离子半径阴离子大于阳离子,具有相同排布的离子原子序数大的离子半径小,故A错误;
B.对于主族元素周期数=电子层数、主族族序数=最外层电子数,故B正确;
C.HF属于弱酸,而HCl属于强酸,氟元素非金属性强于氯元素,但氢氟酸的酸性应弱于盐酸,故C错误;
D.在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素,在过渡元素中可以寻找制备催化剂及耐高温材料的元素,故D错误.
故选:B.
点评 本题考查结构性质位置关系应用,注意对元素周期表与元素周期律的掌握,比较基础,侧重对基础知识的巩固.


科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5 mol/(L•s) | B. | 1.5 mol/(L•s) | C. | 2 mol/(L•s) | D. | 3 mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 负极发生氧化反应 | B. | 正极为电子流入的一极 | ||
| C. | 比较不活泼的金属为负极 | D. | 负极为失去电子的一极 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
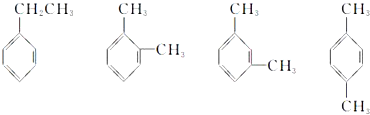
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚稀溶液常用于外科消毒,所以自来水也可以用苯酚进行消毒处理 | |
| B. | 煤经气化和液化两个化学变化过程,可变为清洁能源 | |
| C. | 石油裂解的目的是提高汽油等轻质油的产量和质量 | |
| D. | “神州七号”的防护层中含聚四氟乙烯,聚四氟乙烯属于不饱和烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④⑤③ | B. | ⑥①⑤③ | C. | ⑧①⑦ | D. | ⑧②⑤③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com