
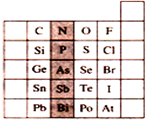
| A. | PH3的沸点比NH3高 | |
| B. | PH3的稳定性比H2S强 | |
| C. | 该纵行元素的最高价氧化物对应的水化物化学式均为H3RO4 | |
| D. | H3AsO4的酸性比H3PO4弱 |
分析 A.氨气分子之间存在氢键,沸点高于PH3的;
B.元素非金属性越强,氢化物越稳定;
C.氮元素最高价氧化物对应的水化物化学式均为HNO3;
D.非金属性越强,最高价含氧酸的酸性越强.
解答 解:A.氨气分子之间存在氢键,PH3分子之间存在范德华力,氢键比范德华力更强,故氨气的沸点高于PH3的,故A错误;
B.同主周期自左而右元素非金属性增强,元素非金属性越强,氢化物越稳定,故PH3的稳定性比H2S弱,故B错误;
C.氮元素最高价氧化物对应的水化物化学式均为HNO3,故C错误;
D.同主族自上而下元素非金属性增强,非金属性越强,最高价含氧酸的酸性越强,故H3AsO4的酸性比H3PO4弱,故D正确,
故选D.
点评 本题考查元素周期律的应用,难度不大,注意理解A选项中氢键对物质性质的影响.


科目:高中化学 来源: 题型:选择题
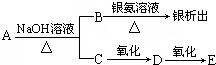
| A. | A可能易溶于水 | B. | B中既有醛基又有羧基 | ||
| C. | C的结构可能是CH3(CH3)2CH2OH | D. | E一定是链状饱和一元酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 +Br2
+Br2
 ,反应类型是加成反应;
,反应类型是加成反应; ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述三种元素的原子半径大小为Y<X<W | |
| B. | W、X、Y原子的核外最外层电子数的总和为10 | |
| C. | 由W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点 | |
| D. | W与Y只能形成含极性共价键的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{94}^{239}$Pu含94个质子 | |
| B. | ${\;}_{94}^{239}$Pu中的中子数和质子数之差为51 | |
| C. | ${\;}_{94}^{239}$Pu中含有94个中子 | |
| D. | ${\;}_{94}^{239}$Pu具有放射性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
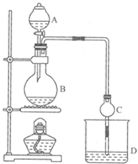 某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸铵,D中放有饱和碳酸钠溶液.
某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸铵,D中放有饱和碳酸钠溶液.| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
 CH3CO18OC2H5+H2O
CH3CO18OC2H5+H2O查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子化合物中只含有离子键 | |
| B. | 共价化合物中可能含离子键 | |
| C. | 含离子键的化合物不一定为离子化合物 | |
| D. | 共价化合物中不含离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com