
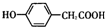
 ;写出A与NaHCO3溶液反应的化学方程式
;写出A与NaHCO3溶液反应的化学方程式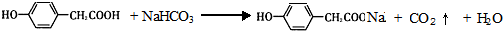 .
. 分析 (1)N(O)=$\frac{152×31.58%}{16}$=3,分子中C、H原子个数比为1:1,则N(CH)=$\frac{152×(1-31.58%)}{13}$=8,以此可确定分子式;
(2)A遇FeCl3溶液显紫色,说明分子中含有酚羟基,A能与NaHCO3溶液反应,说明分子中含有羧基,苯环上的一氯取代物有两种,说明结构对称.
解答 解:(1)N(O)=$\frac{152×31.58%}{16}$=3,分子中C、H原子个数比为1:1,则N(CH)=$\frac{152×(1-31.58%)}{13}$=8,则A的分子式为:C8H8O3,故答案为:C8H8O3;
(2)A分子式为C8H8O3,A遇FeCl3溶液显紫色,说明分子中含有酚羟基,A能与NaHCO3溶液反应,说明分子中含有羧基,苯环上的一氯取代物有两种,说明结构对称,则结构简式应为 ,A与NaHCO3溶液反应的化学方程式为
,A与NaHCO3溶液反应的化学方程式为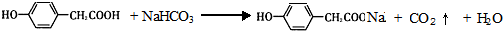 ,
,
故答案为: ;
;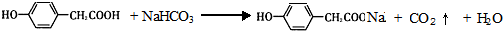 .
.
点评 本题考查有机物的推断,综合考查学生的计算能力、分析能力,答题时注意运用计算和性质相结合推断物质种类,难点是结构简式的书写,题目难度中等.


科目:高中化学 来源: 题型:多选题
| A. | FeS2既是氧化剂又是还原剂 | |
| B. | 被氧化的硫和被还原的硫的质量比为3:7 | |
| C. | 氧化剂只有CuSO4 | |
| D. | 1 mol CuSO4可氧化$\frac{5}{7}$mol的硫 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃、101kPa时,11.2L H2中含有的原子数为NA | |
| B. | 78g Na2O2与足量水充分反应时电子转移数为2NA | |
| C. | 等质量的CO与CO2中所含碳原子数之比为11:7 | |
| D. | 将98g H2SO4溶解于500mL水中,所得溶液中硫酸的物质的量浓度为2 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中的阴离子只有CO32-和OH- | |
| B. | NaHCO3溶液中:c(H+)+c(H2CO3)═c(OH-) | |
| C. | 10 mL0.10 mol•L-1CH3COOH溶液加入等物质的量的NaOH后,溶液中离子的浓度由大到小的顺序是:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| D. | 中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗的NaOH物质的量相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓H2SO4具有强氧化性是因为其中含+6价S,所有只要含最高价+6价S的化合物就具有强氧化性 | |
| B. | H2S中的S处于最低价,因此其不可能具有氧化性 | |
| C. | 浓H2SO4可把Na2SO3氧化 | |
| D. | 因为元素化合价变化以相邻价态之间转化最容易,因此发生氧化还原反应时,浓H2SO4对应的产物一般为SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.lmol•L-lNaHC2O4溶液(pH=5.5):c(Na+)>c( HC2O4-)>c(H2C2O4)>c(C2O42- ) | |
| B. | 0.lmol•L-1NaHS 溶液:C(OH-)+c(S2-)=c( H+)+c(H2S) | |
| C. | 0.lmol•L-1CH3COOH 溶液和 0.lmol•L-1CH3COONa 溶液等体积混合:c(Na+)>c(CH3COOH)>c(CH3COO-)>c(H+)>c( OH-) | |
| D. | 0.lmol•L-lNH4HSO4 溶液中滴加 0.lmol•L-1NaOH 溶液至中性:c(Na+ )>c(SO42- )>c(NH4+ )>c(OH-)=c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com