
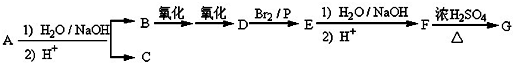

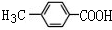
 .
.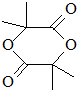 .
.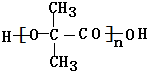 +(n-1)H2O,该反应属于缩聚反应(填反应类型).
+(n-1)H2O,该反应属于缩聚反应(填反应类型). 分析 C的不饱和度=$\frac{8×2+2-8}{2}$=5,C能与碳酸氢钠反应,说明C中含有羧基,且在铁作催化剂下与液溴反应只能生成2种沸点不同的一溴代芳香族化合物,则C结构简式为 ;
;
A水解生成羧酸和醇,C是羧酸,则B是醇,B能连续被氧化生成D,D能发生信息②的反应,A为酯,A中含有2个O原子,则A相对分子质量=$\frac{16×2}{16.7%}$≈192,B相对分子质量=192+18-8×12-8×1-16×2=74,
B为一元醇时,碳原子个数=$\frac{74-16-2}{14}$=4,符合题意,所以B中含有4个碳原子,B能连续被氧化生成羧酸D,D发生取代反应生成E,E发生消去反应生成F,F发生缩聚反应生成G,G的粗产物中,含有六元环状化合物杂质H,经检测H的核磁共振氢谱只有一个峰,则G结构简式为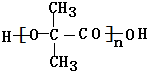 ,H结构简式为
,H结构简式为 ,则B结构简式为(CH3)2CHCH2OH,D结构简式为(CH3)2CHCOOH、E结构简式为(CH3)2CBrCOOH、F结构简式为(CH3)2C(OH)COOH,A结构简式为
,则B结构简式为(CH3)2CHCH2OH,D结构简式为(CH3)2CHCOOH、E结构简式为(CH3)2CBrCOOH、F结构简式为(CH3)2C(OH)COOH,A结构简式为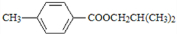 ,据此分析解答.
,据此分析解答.
解答 解:C的不饱和度=$\frac{8×2+2-8}{2}$=5,C能与碳酸氢钠反应,说明C中含有羧基,且在铁作催化剂下与液溴反应只能生成2种沸点不同的一溴代芳香族化合物,则C结构简式为 ;
;
A水解生成羧酸和醇,C是羧酸,则B是醇,B能连续被氧化生成D,D能发生信息②的反应,A为酯,A中含有2个O原子,则A相对分子质量=$\frac{16×2}{16.7%}$≈192,B相对分子质量=192+18-8×12-8×1-16×2=74,
B为一元醇时,碳原子个数=$\frac{74-16-2}{14}$=4,符合题意,所以B中含有4个碳原子,B能连续被氧化生成羧酸D,D发生取代反应生成E,E发生消去反应生成F,F发生缩聚反应生成G,G的粗产物中,含有六元环状化合物杂质H,经检测H的核磁共振氢谱只有一个峰,则G结构简式为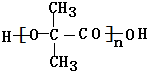 ,H结构简式为
,H结构简式为 ,则B结构简式为(CH3)2CHCH2OH,D结构简式为(CH3)2CHCOOH、E结构简式为(CH3)2CBrCOOH、F结构简式为(CH3)2C(OH)COOH,A结构简式为
,则B结构简式为(CH3)2CHCH2OH,D结构简式为(CH3)2CHCOOH、E结构简式为(CH3)2CBrCOOH、F结构简式为(CH3)2C(OH)COOH,A结构简式为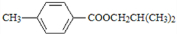 ,
,
(1)通过以上分析知,A分子式为C12H16O2,故答案为:C12H16O2;
(2)C结构简式为 ,故答案为:
,故答案为: ;
;
(3)C为 ,C的同分异构体能发生银镜反应又能发生水解反应,说明含有酯基和醛基,为甲酸酯,取代基为HCOO-、-CH3,有邻间对三种,取代基为HCOOCH2-,有一种,所以符合条件的有4种,故答案为:4;
,C的同分异构体能发生银镜反应又能发生水解反应,说明含有酯基和醛基,为甲酸酯,取代基为HCOO-、-CH3,有邻间对三种,取代基为HCOOCH2-,有一种,所以符合条件的有4种,故答案为:4;
(4)在G的粗产物中,含有六元环状化合物杂质H,经检测H的核磁共振氢谱只有一个峰,则H结构简式为 ,
,
故答案为: ;
;
(5)G结构简式为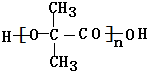 ,F结构简式为(CH3)2C(OH)COOH,F发生缩聚反应生成G,反应类型是缩聚反应,
,F结构简式为(CH3)2C(OH)COOH,F发生缩聚反应生成G,反应类型是缩聚反应,
反应方程式为n(CH3)2C(OH)COOH$\stackrel{一定条件下}{→}$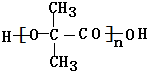 +(n-1)H2O,
+(n-1)H2O,
故答案为:n(CH3)2C(OH)COOH$\stackrel{一定条件下}{→}$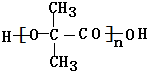 +(n-1)H2O;缩聚反应.
+(n-1)H2O;缩聚反应.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力,正确判断A结构简式是解本题关键,注意结合题给信息采用知识迁移方法进行推断,需要学生熟练掌握基础知识并灵活运用,题目难度中等.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.3mol | B. | 0.4mol | C. | 0.5mol | D. | 0.6mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ②③④ | C. | ②④ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{r(Ca)}{r(Mg)}$ | B. | $\frac{r(C{l}^{-})}{r(A{l}^{3+})}$ | C. | $\frac{r(Na)}{r(Mg)}$ | D. | $\frac{r(N{a}^{+})}{r({F}^{-})}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑦ | B. | ①②③④ | C. | ①③④⑤ | D. | ①④⑥⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
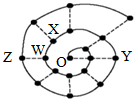 某同学在研究前18号元素时发现,可以将它们排成如下图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中O点(最中心的点)代表起点元素.下列说法中正确的是( )
某同学在研究前18号元素时发现,可以将它们排成如下图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中O点(最中心的点)代表起点元素.下列说法中正确的是( )| A. | 物质YO可能具有较强的氧化性 | |
| B. | 图中离O点越远的元素,其原子半径一定越大 | |
| C. | O2X、WO3分子内都含有氢键,所以沸点都较高 | |
| D. | 科学家发现一种新细菌的DNA链中有砷(As)元素,该As元素最有可能取代了普通DNA链中的Z元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠属于危化品中的易燃固体,其着火时不能用水灭火 | |
| B. | 氰化钠( NaCN)是一种剧毒危险品,其水溶液呈碱性 | |
| C. | 实验室里可将少量的钠保存于煤油中 | |
| D. | NH4N03、NaCN、CaC2中均含有离子键和非极性共价键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com