
【题目】用3g块状大理石与30mL3mol/L盐酸反应制取CO2气体,若要增大反应速率,可采取的措施是( )
①再加入30mL1mol/L盐酸 ②改用30mL6mol/L盐酸 ③改用3g粉末状大理石 ④适当升高温度
A. ①②④ B. ②③④ C. ①③④ D. ①②③
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去)。则W、X不可能是( )
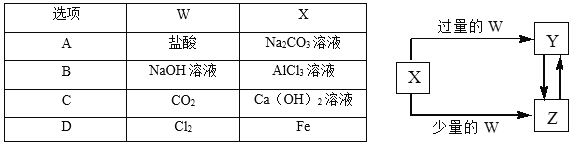
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高分子材料PET聚酯树脂和PMMA的合成路线如下:

已知:  (R、R′代表烃基)
(R、R′代表烃基)
(1)①的反应类型是____________________。
(2)②的化学方程式为________________________________________。
(3)F的核磁共振氢谱显示只有一组峰,⑤的化学方程式为____________。
(4)G的结构简式为____________________。
(5)⑦的化学方程式为______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.胶体都有丁达尔现象B.向FeCl3溶液中加入KSCN,最终会看到血红色沉淀
C.氢氧化铁胶体可以透过滤纸D.向硫酸铜溶液中加入一小块金属钠,最终会看到蓝色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合溶液中可能含有HCl、MgCl2、AlCl3、NH4Cl、Na2CO3、KCl中的几种物质,往该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入的NaOH溶液体积(V)的关系如图所示。回答下列问题:
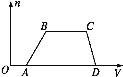
(1)溶液中一定含有的溶质是______________________(填化学式)。
(2)溶液中一定不含有的溶质是________________(填化学式)。
(3)溶液中可能含有的溶质是____(填名称),判断该物质是否存在的实验方法是____,若存在则现象是_______________________________________________。
(4)分别写出AB段、BC段发生反应的离子方程式:
①AB段为_______________________________________________________________;
②BC段为_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
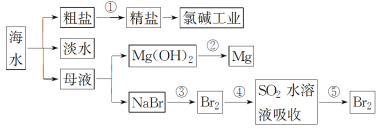
(1)过程①是为了除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,若要除去SO42-,则需要加入的试剂为_____________;若所加的该试剂过量,则可以被后加入的________________除去。
(2)过程②能否一步实现转化?______________(填“能”或“否”),Mg(OH)2与盐酸反应可以得到MgCl2溶液,则该反应的离子方程式为_____________________________________________。
(3)过程④反应的离子方程式为_____________________________________________________。
(4)若用CCl4萃取溴水中的Br2,分液时CCl4层应从分液漏斗的_____________放出。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某第三周期元素X的气态氢化物的化学式为XH3,则X的最高价氧化物的水化物的化学式为( )
A. H2XO3 B. HXO3 C. H3XO4 D. H2XO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国利用合成气直接制烯烃获重大突破,其原理是
反应①:C(s)+1/2O2(g) = CO(g) ΔH1
反应②:C(s)+H2O(g) = CO(g)+H2(g) ΔH2
反应③:CO(g)+2H2(g) = CH3OH(g) ΔH3=-90.1 kJ·mol-1
反应④:2CH3OH(g) = CH3OCH3(g)+H2O(g) ΔH4,能量变化如图所示
反应⑤:3CH3OH(g)= CH3CH=CH2(g)+3H2O(g) ΔH5=-31.0 kJ·mol-1
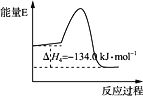
下列说法正确的是
A. 反应③使用催化剂,ΔH3减小
B. 反应④中正反应的活化能大于逆反应的活化能
C. ΔH1-ΔH2<0
D. 反应①和反应②,制取等量的CO,无论哪种途径,消耗的能量均相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com