
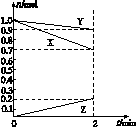
某温度时,在2L容器中,X,Y,Z三种物质的物质的量随时间变化的曲线如图所示。由图中数据分析:该反应的化学方程式为____________。反应开始至2 min,用Z表示的平均反应速率为________。
思路分析:看清图中横、纵坐标的含义及曲线的变化趋势,抓住起点、终点、最高点、最低点、转折点等进行综合分析。
解析:由图可知,X、Y的物质的量随反应的进行而减小,Z的物质的量随反应的进行而增大,则X和Y为反应物,Z为生成物。Δn(X)=1.0 mol-0.7 mol=0.3 mol,Δn(Y)=1.0 mol-0.9 mol=0.1 mol,Δn(Z)=0.2 mol-0 mol=0.2 mol,Δn(X)∶Δn(Y)∶Δn(Z)=0.3 mol∶0.1 mol∶0.2 mol=3∶1∶2,故反应方程式为3X+Y===2Z。v(Z)=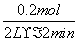 =0.05 mol·L-1·min-1。
=0.05 mol·L-1·min-1。
答案:3X+Y===2Z 0.05 mol·L-1·min-1


 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源: 题型:
盐酸、醋酸和碳酸氢钠是生活中常见的物质。下列表述正确的是( )
A.在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中的阴离子只有CO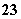 和OH-
和OH-
B.NaHCO3溶液中:[H+]+[H2CO3]=[OH-]
C.10 mL 0.10 mol·L-1 CH3COOH溶液加入等物质的量的NaOH后,溶液中离子的浓度由大到小的顺序是:[Na+]>[CH3COO-]>[OH-]>[H+]
D.中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗的NaOH物质的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
将0.2 mol·L-1 HA溶液与0.2 mol·L-1 NaOH溶液等体积混合,测得混合溶液中[Na+]>[A-],则(用“>”、“<”或“=”填写下列空白):
(1)混合溶液中[HA]________[A-];
(2)混合溶液中[HA]+[A-]________0.1 mol·L-1;
(3)混合溶液中由水电离出的[OH-]______0.2 mol·L-1 HA溶液中由水电离出的[H+];
(4)25℃时,如果取0.2 mol·L-1 HA溶液与0.1 mol·L-1 NaOH溶液等体积混合,测得混合溶液的pH<7,则HA的电离程度________NaA的水解程度。
查看答案和解析>>
科目:高中化学 来源: 题型:
如下图所示,实线表示放热反应X(g)+Y(g)Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按虚线进行,可采取的措施是( )
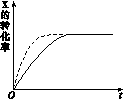
A.升高温度 B.加大X的投入量
C.加催化剂 D.增大体积
查看答案和解析>>
科目:高中化学 来源: 题型:
酸蒸气能形成二聚分子:2CH3COOH(g)(CH3COOH)2(g) ΔH<0。现欲测定乙酸的相对分子质量,应采用的条件为( )
A.高温、低压 B.低温、高压
C.低温、低压 D.高温、高压
查看答案和解析>>
科目:高中化学 来源: 题型:
在溶液中,反应A+2BC分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100 mol/L、c(B)=0.200 mol/L及c(C)=0 mol/L。反应物A的浓度随时间的变化如下图所示。

请回答下列问题:
(1)与①比较,②和③分别仅改变一种反应条件。所改变的条件和判断的理由是:
②________________________________________________________________________。
③________________________________________________________________________。
(2)实验②平衡时B的转化率为________;实验③平衡时C的浓度为________;
(3)该反应的ΔH________0。其判断理由是________________________________________________________________________________________________________________________________________________
(4)该反应进行到4.0 min 时的平均反应速率:
实验②:vB=___________________;
实验③:vC=___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有X、Y、Z、M四种元素均为短周期元素。有关信息如下表:
| 原子或分子结构、单质或化合物相关信息 | |
| X | 含X元素的物质焰颜色反应为黄色 |
| Y | 单质为双原子分子。若低温蒸发液态空气,因其沸点较低可先获得Y的单质 |
| Z | Z元素原子易失去2个电子形成8电子结构的离子 |
| M | M元素原子的最外层电子数是K层电子数的3倍,M与X处于同一周期 |
(1)X元素在周期表的位置是 ▲ ;
(2)1个Y单质分子中含 ▲ 对个共用电子对;
(3)Z能在CO2气体中燃烧,其化学反应方程式为 ▲ 。
(4)化合物X2M溶液在空气中长期放置,与氧气反应会生成与过氧化钠的结构和化学性质相似的物质X2M2,其溶液显黄色.则X2M2的电子式为 ▲ ,用化学方程式表示X2M溶液在空气中的变质过程 ▲ .
查看答案和解析>>
科目:高中化学 来源: 题型:
为了净化和收集由盐酸和大理石制得的CO2气体,从下图中选择合适的装置并连接。合理的是( )
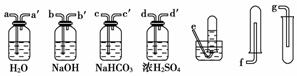
A.a—a′→d—d′→e B.b—b′→d—d′→g
C.c—c′→d—d′→g D.d—d′→c—c′→f
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com