
在恒温、恒容下,当反应容器内总压强不随时间变化时,下列可逆反应一定达到平衡的是( )
A.A(g)+B(g)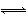 C(g)B.A(g)+2B(g)
C(g)B.A(g)+2B(g) 3C(g)
3C(g)
C.A(g)+B(g) C(g)+D(g)D.以上都达到平衡
C(g)+D(g)D.以上都达到平衡
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源:2014年高二化学苏教版选修2 2.2氯碱生产练习卷(解析版) 题型:选择题
下列关于离子交换膜电解槽的叙述,错误的是( )。
A.精制的饱和食盐水进入阳极室
B.纯水(加少量NaOH)进入阴极室
C.阴极产物为NaOH和氢气
D.电解槽的阳极用金属铁网制成
查看答案和解析>>
科目:高中化学 来源:2014年高二化学苏教版选修2 1.1水的净化与污水处理练习卷(解析版) 题型:填空题
请你参与下列问题的探究:
(1)三峡工程二期已经开始蓄水,为防止三峡库区水被污染,应该采取的措施是________(填序号)。
①清理蓄水库底废弃物
②防止船舶污染
③整治相关河流污染
④治理库区和上游工业污染
(2)载人飞船须建立水的循环体系,以保证宇航员的生活用水并减少飞船的携水量。请将图中各项用箭头连接成水的循环系统(注:氢氧燃料电池反应产生电能,同时生成水)。
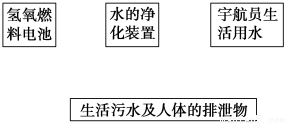
(3)日常生活中我们要科学合理地节约用水,有一个水龙头,每秒漏水2滴,则一天漏水________g(平均每20滴为1 mL,水的密度为1 g·mL-1)。若每个人每日补充水2.5 L,则这些水可以给一个人补充________天水。(计算结果精确到0.1)
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 8化学平衡移动练习卷(解析版) 题型:选择题
对处于平衡状态的反应:2A(g)+B(g)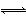 2C(g)(已知反应为放热反应),下列叙述正确的是( )
2C(g)(已知反应为放热反应),下列叙述正确的是( )
A.增大压强,v(正)增大,v(逆)减小
B.升高温度,v(正)减小,v(逆)增大
C.增大A浓度的瞬间,v(正)增大,v(逆)不变
D.增大A浓度的瞬间,v(正)增大而v(逆)减小
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 7化学平衡状态的建立及标志练习卷(解析版) 题型:选择题
一定条件下,发生如下反应:2A(g)+2B(g)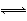 3C(g)+ D(g)在容积不变的密闭容器中进行,达到化学平衡状态的标志是( )
3C(g)+ D(g)在容积不变的密闭容器中进行,达到化学平衡状态的标志是( )
A.单位时间内生成n mol B,同时消耗3n mol C
B.容器内压强不随时间而变化
C.混合气体的密度不随时间变化
D.单位时间内生成2n mol A,同时生成n mol D
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 6影响化学反应速率的因素练习卷(解析版) 题型:填空题
用如图所示装置进行如下实验:
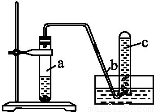
(1)在检查装置的气密性后,向试管a中加入10 mL 6 mol·L-1的稀硝酸和1 g铜片,立即用带有导管的橡皮塞塞紧试管口。请写出在试管a中有可能发生的所有反应的化学方程式 。
(2)在实验过程中常常反应开始时速率缓慢,随后逐渐加快,这是由于 ,当反应进行一段时间后速率又逐渐减慢,原因是 。
(3)欲较快地制得NO,可采取的措施是 (填写字母序号)。
A.加热B.使用铜粉C.稀释HNO3D.增大硝酸的浓度
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 6影响化学反应速率的因素练习卷(解析版) 题型:选择题
反应C(s)+H2O(g)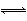 CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
A.增加C的量
B.将容器的体积缩小一半
C.保持体积不变,充入H2O(g)使体系压强增大
D.保持压强不变,充入N2使容器体积变大
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 4化学反应热的计算练习卷(解析版) 题型:填空题
把煤作为燃料可通过下列两种途径:
途径Ⅰ C(s)+O2(g) CO2(g) ΔH1<0①
CO2(g) ΔH1<0①
途径Ⅱ 先制成水煤气:
C(s)+H2O(g) CO(g)+H2(g) ΔH2>0②
CO(g)+H2(g) ΔH2>0②
再燃烧水煤气:
2CO(g)+O2(g) 2CO2(g) ΔH3<0③
2CO2(g) ΔH3<0③
2H2(g)+O2(g) 2H2O(g) ΔH4<0④
2H2O(g) ΔH4<0④
请回答下列问题:
(1)途径Ⅰ放出的热量理论上 (填“大于”“等于”或“小于”)途径Ⅱ放出的热量。
(2)ΔH1、ΔH2、ΔH3、ΔH4的数学关系式是 。
(3)已知:①C(s)+O2(g) CO2(g) ΔH1=-393.5 kJ·mol-1
CO2(g) ΔH1=-393.5 kJ·mol-1
②2CO(g)+O2(g) 2CO2(g) ΔH2=-566 kJ·mol-1
2CO2(g) ΔH2=-566 kJ·mol-1
③TiO2(s)+2Cl2(g) TiCl4(s)+O2(g) ΔH3=+141 kJ·mol-1
TiCl4(s)+O2(g) ΔH3=+141 kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s) TiCl4(s)+2CO(g)的ΔH= 。
TiCl4(s)+2CO(g)的ΔH= 。
(4)已知下列各组热化学方程式
①Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) ΔH1=-25 kJ·mol-1
2Fe(s)+3CO2(g) ΔH1=-25 kJ·mol-1
②3Fe2O3(s)+CO(g) 2Fe3O4(s)+CO2(g) ΔH2=-47 kJ·mol-1
2Fe3O4(s)+CO2(g) ΔH2=-47 kJ·mol-1
③Fe3O4(s)+CO(g) 3FeO(s)+CO2(g) ΔH3=+640 kJ·mol-1
3FeO(s)+CO2(g) ΔH3=+640 kJ·mol-1
请写出FeO(s)被CO(g)还原成Fe和CO2(g)的热化学方程式 ______________________。
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 21电解原理练习卷(解析版) 题型:选择题
若某电能与化学能的转化装置(电解池或原电池)中发生的总反应的离子方程式是Cu+2H+ Cu2++H2↑,则下列关于该装置的有关说法中正确的是( )
Cu2++H2↑,则下列关于该装置的有关说法中正确的是( )
A.该装置可能是原电池,也可能是电解池
B.该装置只能是原电池,且电解质溶液为硝酸
C.该装置只能是电解池,且金属铜为该电解池的阳极
D.该装置只能是原电池,电解质溶液不可能是盐酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com