
A.SiO2 B.NaCl C.CCl4固体 D.KOH
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
 下列关于晶体说法的正确组合是( )
下列关于晶体说法的正确组合是( )查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
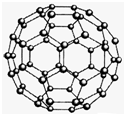 (2010?济南二模)【化学-物质结构与性质】
(2010?济南二模)【化学-物质结构与性质】查看答案和解析>>
科目:高中化学 来源: 题型:
 下列关于晶体的说法正确的组合是( )
下列关于晶体的说法正确的组合是( )| A、①②③⑥ | B、①②④ | C、③⑤⑦ | D、③⑤⑧ |
查看答案和解析>>
科目:高中化学 来源:2012届江苏省高二下学期期末考试化学试题 题型:选择题
下列关于晶体的说法正确的组合是( )
①分子晶体中都存在共价键 [来源:学*科*网]
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低
④离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键
⑤CaTiO3晶体中(晶胞结构如图所示)每个Ti4+和12个O2-相紧邻
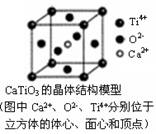
⑥SiO2晶体中每个硅原子与两个氧原子以共价键相结合
⑦晶体中分子间作用力越大,分子越稳定
⑧氯化钠熔化时离子键被破坏
A.①②③⑥ B.①②④ C.③⑤⑦ D.③⑤⑧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com