
【题目】下列各项中所列举的物质与所属类别对应不正确的是
A.酸性氧化物:CO2、SO2、SiO2、Cl2O7
B.非电解质:蔗糖、四氯化碳、氨气、氯气
C.同素异形体:石墨与金刚石、单斜硫与斜方硫
D.混合物:铝热剂、纯净矿泉水、水玻璃、焦炉气
科目:高中化学 来源: 题型:
【题目】现有AlCl3和MgSO4混合溶液,向其中不断加入0.1mol/L 的NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl﹣与SO42﹣的物质的量之比为( ) 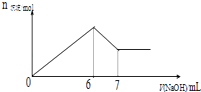
A.2:1
B.2:3
C.6:1
D.3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A. 2NO(g)+2CO(g)=N2(g)+2CO2(g)在常温下能自发进行,则该反应的△H>0
B. 对于乙酸与乙醇的酯化反应(△H<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大
C. CH3COOH 溶液加水稀释后,溶液中![]() 的值增大
的值增大
D. Na2CO3溶液中加入少量Ca(OH)2 固体,CO32-水解向左移动,溶液的pH 增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验不能证明一元酸HR为弱酸的是( )
A.室温下,NaR溶液的pH大于7
B.HR溶液加入少量NaR固体,溶解后溶液的pH变大
C.HR溶液的导电性比盐酸弱
D.0.01mol·L-1的HR溶液pH=2.8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水的电离平衡曲线如图所示,下列说法不正确的是

A. 图中五点Kw间的关系:B>C>A=D=E
B. 若从A点到D点,可采用在水中加入少量酸的方法
C. 若从A点到C点,在温度不变时向水中加入适量NH4Cl固体
D. 若处在B点时,将pH=2的硫酸与pH=10的KOH溶液等体积混合后,溶液显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁和铁合金是生产、生活中常用的材料,下列说法中错误的是
A.不锈钢比生铁抗腐蚀能力强
B.以铁为阴极、铜片为阳极、硫酸铜为电镀液可以实现铁制品镀铜
C.铁与稀硫酸反应,铁与浓硫酸不能反应
D.铁轨焊接时可以用铝热反应的方法制取少量的铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】700 ℃时,向容积为2 L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g) ![]() CO2(g)+H2(g) 反应过程中测定的部分数据见下表(表中t2>t1):
CO2(g)+H2(g) 反应过程中测定的部分数据见下表(表中t2>t1):
反应时间/min | n(CO)/mol | n(H2O)/mol |
0 | 1.20 | 0.60 |
t1 | 0.80 | |
t2 | 0.20 |
下列说法正确的是 ( )
A. 反应在t1 min内的平均速率为v(H2)=![]() mol·L-1·min-1
mol·L-1·min-1
B. 保持其他条件不变,起始时向容器中充入0.60 mol CO和1.20 mol H2O,达到平衡时n(CO2)=0.30 mol
C. 保持其他条件不变,向平衡体系中再通入0.20 mol H2O,与原平衡相比,达到新平衡时CO转化率增大,H2O的体积分数增大
D. 温度升高至800 ℃,上述反应平衡常数为0.64,则正反应为吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下表中烃的分子式排布规律,判断空格中烃的同分异构体数目是
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
CH4 | C2H4 | C3H8 | C4H8 | C6H12 | C7H16 | C8H16 |
A. 3 B. 4 C. 5 D. 6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化物是形成光化学烟雾和酸雨的重要原因。回答下列问题:
(1)光化学烟雾的产生机理(R为烃基)及烟雾箱(添加有NO和丙烯的空气,并用紫外光照射)中部分物质的浓度随照射时间的变化如图所示。

①80min后NO2浓度减小,是由于发生了反应______(填“I”“Ⅱ”“Ⅲ”或“Ⅳ”,下同),O3开始产生并明显增多,是由于发生了反应_______。
②0~50 min内,v(NO)=______mL·m-3·min-l。
③烟雾箱中丙烯与O2、NO反应会生成甲醛、乙醛及NO2,总反应的化学方程式为_______。
(2)处理含氮氧化物(NO和NO2)烟气的常用方法是碱液吸收法,用质量分数为2%的NaOH溶液吸收不同氧化度[氧化度![]() ,NO氧化度可看作0,NO2氧化度可看作100%]的氮氧化物,其吸收率随时间的变化如图所示。
,NO氧化度可看作0,NO2氧化度可看作100%]的氮氧化物,其吸收率随时间的变化如图所示。

①从反应速率与吸收率得出的结论是___________。
②a=50%时,碱液吸收的离子方程式为___________。
③a=70%时,吸收得到的盐是___________(填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com