
| A£® | NH3 | B£® | SO2 | C£® | Na | D£® | NO |
·ÖĪö ³£ĪĀĻĀÓėĖ®·“Ó¦µÄĪļÖŹÓŠ»īĘĆ¼ī½šŹōµ„ÖŹŅŌ¼°¶ŌÓ¦µÄŃõ»ÆĪļ£¬Ņ×ČÜÓŚĖ®µÄĖįŠŌŃõ»ÆĪļŅŌ¼°æÉÓėĖ®·¢ÉśŃõ»Æ»¹Ō·“Ó¦µÄ·Ē½šŹōŠŌŃõ»ÆĪļ£¬°±ĘųµČ£¬ŅŌ“Ė½ā“šøĆĢā£®
½ā“š ½ā£ŗA£®°±ĘųæÉÓėĖ®·“Ӧɜ³ÉŅ»Ė®ŗĻ°±£¬¹ŹA²»Ń”£»
B£®¶žŃõ»ÆĮņÓėĖ®·“Ӧɜ³ÉŃĒĮņĖį£¬¹ŹB²»Ń”£»
C£®ÄĘŗĶĖ®·“Ӧɜ³ÉĒāŃõ»ÆÄĘŗĶĒāĘų£¬¹ŹC²»Ń”£»
D£®NO²»ŗĶĖ®·“Ó¦£¬¹ŹDŃ”£®
¹ŹŃ”D£®
µćĘĄ ±¾Ģā×ŪŗĻæ¼²éŌŖĖŲ»ÆŗĻĪļÖŖŹ¶£¬ĪŖøßĘµæ¼µć£¬²ąÖŲæ¼²éѧɜµÄ·ÖĪöÄÜĮ¦ŗĶĖ«»łÖŖŹ¶£¬ÄŃ¶Č²»“ó£¬×¢ŅāĻą¹Ų»ł“”ÖŖŹ¶µÄ»żĄŪ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĆŗµÄŅŗ»Æ | B£® | ŗ£Ė®É¹ŃĪ | C£® | ĄÆÖņÕÕĆ÷ | D£® | ŹÆÓĶĮŃ½ā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·Ö×Ó¾§ĢåÖŠŅ»¶Øŗ¬ÓŠ¹²¼Ū¼ü£¬²»ŗ¬ÓŠĄė×Ó¼ü | |
| B£® | ½öŗ¬¹²¼Ū¼üµÄĪļÖŹ²»Ņ»¶ØŹĒ¹²¼Ū»ÆŗĻĪļ | |
| C£® | Ō×Ó¾§ĢåÖŠÖ»“ęŌŚ·Ē¼«ŠŌ¹²¼Ū¼ü | |
| D£® | ²»Ķ¬Ō×ÓŠĪ³ÉµÄ“æ¾»ĪļŅ»¶ØŹĒ»ÆŗĻĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČÜŅŗ | B£® | Čé×ĒŅŗ | C£® | ½ŗĢå | D£® | Šü×ĒŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1.0mol•L-1 KNO3ČÜŅŗ£ŗH+”¢Fe2+”¢Cl-”¢SO42- | |
| B£® | ÓėĀĮ·Ū·“Ó¦·Å³öĒāĘųµÄĪŽÉ«ČÜŅŗÖŠ£ŗNO3-”¢Mg2+”¢Na+”¢SO42- | |
| C£® | ŌŚĪŽÉ«ĶøĆ÷ČÜŅŗÖŠ£ŗBa2+”¢Ca2+”¢NO3-”¢Cl- | |
| D£® | 0.1 mol•L-1 FeCl3ČÜŅŗ£ŗK+”¢NH+4”¢I-”¢SCN- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
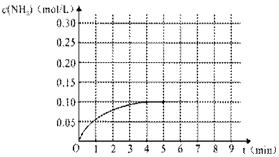 ŌŚŅ»ČŻ»żĪŖ2LµÄĆܱÕČŻĘ÷ÄŚ¼ÓČė0.2molµÄN2ŗĶ0.6molµÄH2£¬ŌŚŅ»¶ØĢõ¼žĻĀ·¢ÉśČēĻĀ·“Ó¦£ŗN2£Øg£©+3H2£Øg£©?2NH3£Øg £©”÷H£¼0£¬·“Ó¦ÖŠNH3µÄĪļÖŹµÄĮæÅØ¶ČµÄ±ä»ÆµÄĒéæöČēĶ¼£ŗ
ŌŚŅ»ČŻ»żĪŖ2LµÄĆܱÕČŻĘ÷ÄŚ¼ÓČė0.2molµÄN2ŗĶ0.6molµÄH2£¬ŌŚŅ»¶ØĢõ¼žĻĀ·¢ÉśČēĻĀ·“Ó¦£ŗN2£Øg£©+3H2£Øg£©?2NH3£Øg £©”÷H£¼0£¬·“Ó¦ÖŠNH3µÄĪļÖŹµÄĮæÅØ¶ČµÄ±ä»ÆµÄĒéæöČēĶ¼£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³Ź¼īŠŌ | B£® | ³ŹĖįŠŌ | C£® | ³ŹÖŠŠŌ | D£® | c£ØH+£©=c£ØOH-£© |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com