
在常温下,下列五种溶液:①0.1 mol·L-1 NH4Cl ②0.1 mol·L-1 CH3COONH4
③0.1 mol·L-1 NH4HSO4 ④0.1 mol·L-1 NH3·H2O和0.1 mol·L-1 NH4Cl混合液
⑤0.1 mol·L-1 NH3·H2O。
请根据要求填写下列空白:
(1)溶液①呈________性(填“酸”、“碱”或“中”),其原因是________________________(用离子方程式表示)。
(2)在上述五种溶液中,pH最小的是________;c(NH )最小的是________(填序号)。
)最小的是________(填序号)。
(3)比较溶液②、③中c(NH )的大小关系是②________③(填“>”“<”或“=”)。
)的大小关系是②________③(填“>”“<”或“=”)。
(4)在溶液④中,__________的浓度为0.1 mol·L-1;NH3·H2O和__________的物质的量浓度之和为0.2 mol·L-1。
(5)常温下,测得溶液②的pH=7,则说明CH3COO-的水解程度________(填“>”“<”或“=”)NH 的水解程度,CH3COO-与NH
的水解程度,CH3COO-与NH 浓度的大小关系是:c(CH3COO-)________c(NH
浓度的大小关系是:c(CH3COO-)________c(NH )(填“>”“<”或“=”)。
)(填“>”“<”或“=”)。
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
某无色溶液只可能含有以下几种离子:①Mg2+、②Al3+、③Fe2+、④H+、⑤HCO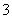 、⑥Cl-、⑦OH-。向其中缓慢地滴入NaOH溶液至过量,产生沉淀的质量与加入NaOH溶液的体积的关系如图所示,由此可确定原溶液中一定含有的离子是( )
、⑥Cl-、⑦OH-。向其中缓慢地滴入NaOH溶液至过量,产生沉淀的质量与加入NaOH溶液的体积的关系如图所示,由此可确定原溶液中一定含有的离子是( )
A.①②⑤ B.①③④
C.②⑥⑦ D.①②④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
为了除去MgCl2酸性溶液中的Fe3+,可在加热搅拌的条件下加入一种试剂,过滤后,再加入适量的HCl,这种试剂是( )
A.NH3·H2O B.NaOH C.Na2CO3 D.MgCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
1下列说法正确的是( )
A.若NaA、NaB溶液的pH分别为9和8,则酸性一定是HA<HB;
B. CH3COONa水解产生CH3COOH和OH-,向水解液中加入少量冰醋酸会因其中和OH-而使水解平衡右移;
C.中和pH和体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同
D.因Al3++3H2O 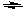 Al(OH)3+3H+,为抑制水解,配制AlCl3溶液时需将AlCl3溶解在稀盐酸中;
Al(OH)3+3H+,为抑制水解,配制AlCl3溶液时需将AlCl3溶解在稀盐酸中;
查看答案和解析>>
科目:高中化学 来源: 题型:
将20mL0.4mol/L硝酸铵溶液跟50mL0.1mol/L氢氧化钡溶液混合,则混合溶液中粒子浓度间的关系正确的是( )
A.c(NO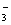 )>c(OH-)>c(NH
)>c(OH-)>c(NH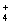 )>c(Ba2+) B.c(NO
)>c(Ba2+) B.c(NO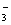 )>c(Ba2+)>c(NH
)>c(Ba2+)>c(NH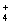 )>c(OH-)
)>c(OH-)
C.c(NO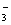 )=c(NH
)=c(NH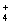 )+c(NH3·H2O)+c(NH3) D.2c(Ba2+)+c(H+)=c(NO
)+c(NH3·H2O)+c(NH3) D.2c(Ba2+)+c(H+)=c(NO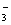 )+c(OH-)
)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
下表各组物质中,物质之间不可能实现如图所示转化的是( )




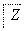
| 选项 | X | Y | Z | M |
| A | NH3 | NO | NO2 | O2 |
| B | Cl2 | FeCl3 | FeCl2 | Fe |
| C | Al | Al(OH)3 | NaAlO2 | NaOH |
| D | NaOH | Na2CO3 | NaHCO3 | CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
铁及其化合物与生产、生活关系密切。
用废铁皮制取铁红(Fe2O3)的部分流程示意图如下:
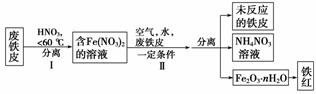
①步骤Ⅰ若温度过高,将导致硝酸分解。硝酸分解的化学方程式为________________________________________________________________________。
②步骤Ⅱ中发生反应:4Fe(NO3)2+O2+(2n+4)H2O===2Fe2O3·nH2O+8HNO3,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,该反应的化学方程式为
________________________________________________________________________。
③上述生产流程中,能体现“绿色化学”思想的是______(任写一项)。
查看答案和解析>>
科目:高中化学 来源: 题型:
以熔融Li2CO3和K2CO3为电解质,天然气经重整催化作用提供反应气的燃料电池如右图。下列说法正确的是
A.以此电池为电源电解精炼铜,当有0.1 mol e- 转移时,有3.2 g铜溶解
B.若以甲烷为燃料气时负极极反应式:
CH4+5O2--8e-=CO32-+2H2O
C.该电池使用过程中需补充Li2CO3和K2CO3
D.空气极发生的电极反应式为
O2+4e-+2CO2===2CO
查看答案和解析>>
科目:高中化学 来源: 题型:
下列现象或应用不能用胶体的知识解释的是( )
A.肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗
B.土壤表面积巨大且一般带负电,能吸收NH4+等营养离子,使土壤具有保肥能力
C.水泥、冶金工厂常用高压电除去工厂烟尘,减少对空气的污染
D.氯化铝溶液中加入碳酸钠溶液会出现白色沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com