
在某100mL混合溶液中,硝酸和硫酸的物质的量浓度分别为0.4mol/L和0.1mol/L,向该混合溶液中加入1.92克铜粉,加热待充分反应后,所得溶液中的Cu2+的物质的量浓度(mol/L)是( )
A.0.15 B.0.225 C.0.35 D.0.45
B
【解析】
试题分析:1.92g铜的物质的量是1.92g÷64g/mol=0.03mol,硝酸和硫酸的物质的量分别是0.04mol和0.01mol,则溶液中氢离子的物质的量是0.06mol,根据反应的离子方程式可知:
3Cu + 8H+ + 2NO3-=3Cu2++4H2O+2NO↑
3mol 8mol 2mol
0.03mol 0.06mol 0.04mol
所以反应中氢离子是不足的,因此铜剩余,所以铜离子的物质的量是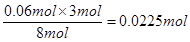 ,因此铜离子的浓度是0.0225mol÷0.1L=0.225mol/L,答案选B。
,因此铜离子的浓度是0.0225mol÷0.1L=0.225mol/L,答案选B。
考点:考查金属铜和硝酸反应的有关计算
点评:该题是高考中的常见题型,难度较大。该题的关键是判断离子的过量问题,采用的方法是根据离子方程式,而不是化学方程式。本题有利于培养学生的逻辑思维能力,以及灵活应变能力。


 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:阅读理解
| 2n-7 |
| 2n+1 |
| 2n-7 |
| 2n+1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:活题巧解巧练·高考化学(第一轮) 题型:022
在某温度下,重水(D2O)的离子积常数为1×10-12,若用pH一样的定义来规定pD,则pD=-lgc(D+).则该温度下:
(1)重水的pD=________.
(2)1L溶有0.01mol的NaOD的D2O溶液,其pD=________.
(3)100mL 0.1mol/L的D2SO4的D2O溶液与100mL 0.4mol/L的KOD的D2O溶液混合后,pD=________.
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
将MgCl2溶液加入NaOH和Na2CO3的混合溶液中,溶液中的离子反应如下:先发生Mg2++2OH-===Mg(OH)2↓,后发生Mg2++CO![]() ===MgCO3↓;经查溶解度表得知, Mg(OH)2的溶解度小于MgCO3的溶解度。在溶解度表中有这样一组数据,表示四种物质在水中、液氨中的溶解度(g溶质/100 g溶剂),如下表:
===MgCO3↓;经查溶解度表得知, Mg(OH)2的溶解度小于MgCO3的溶解度。在溶解度表中有这样一组数据,表示四种物质在水中、液氨中的溶解度(g溶质/100 g溶剂),如下表:
| 溶质 溶剂 | AgNO3 | Ba(NO3)2 | AgCl | BaCl2 |
| 水 | 170 | 9.3 | 1.5×10-4 | 33.3 |
| 液氨 | 86 | 97.2 | 0.8 | 0 |
(1)分别是1.0 mol· L-1的Ag+、Ba2+、NO![]() 和Cl-在水中发生反应的离子方程式是______________________________________________________________。
和Cl-在水中发生反应的离子方程式是______________________________________________________________。
(2)分别是0.50 mol· L-1的以上四种离子在液氨中发生反应的离子方程式是__________________________________________________。
II(6分)、某100mL溶液中含有的部分离子浓度大小如图所示,该溶液可能还含有
 Fe3+、Ba2+、K+、OH-、NO3-、
Fe3+、Ba2+、K+、OH-、NO3-、![]() 、
、![]() 。为了进一步确认,对该溶液进行实验检测:
。为了进一步确认,对该溶液进行实验检测:
①仔细观察,该溶液呈无色、透明、均一状态。
②向100mL溶液中滴入稀硫酸,有23.3g白色沉淀产生,再加稀硝酸,白色沉淀不消失。回答下列问题:由此可知,除了含有Na+、Mg2+、Cl-外,该溶液中肯定还含有的离子及其物质的量浓度为___________,肯定没有的离子是___________,可能含有的离子是___________。
III(6分).试样X由氧化亚铁和氧化铜组成。取质量相等的两份试样进行下图所示实验:

(1)写出步骤③发生的全部反应的离子方程式。
(2)若Y和Z充分反应,生成的不溶物的质量是m,则每份试样X中氧化铜的质量为 (用m表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com