
【题目】对于常温下pH=2的醋酸溶液,下列叙述正确的是
A.c(H+)=c(CH3COO-)
B.加水稀释时![]() 增大
增大
C.与pH = 12的NaOH溶液等体积混合后,溶液呈中性
D.加入醋酸钠固体可抑制醋酸的电离,电离常数Ka变小
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列各组物质中,第一种是混合物,第二种是盐,第三种是酸的是
A. 空气、硫酸铜、硫酸 B. 水、空气、纯碱
C. 食盐水、硝酸、烧碱 D. 氧化铁、胆矾、熟石灰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2和I2在一定条件下能发生反应H2(g)+I2(g)![]() 2HI (g) △H=-a kJmol-1,已知:
2HI (g) △H=-a kJmol-1,已知:

下列说法不正确的是
A. 反应物的总能量高于生成物的总能量
B. 向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2a kJ
C. 断开2 mol H-I键所需能量约为(c+b+a) kJ
D. 断开1 mol H-H键和1 mol I-I键所需能量大于断开2 mol H-I键所需能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】—定温度下,下列溶液的离子浓度关系式正确的是( )
A. pH=5 的H2S溶液中,c(H+)>c(HS-)=1×10-5mol/L
B. 将等物质的量的Na2CO3和NaHCO3混合溶于水中:![]()
C. pH之和为14的H2C2O4与NaOH 溶液混合:c(Na+)>c(H+)>c(OH-)>c(HC2O4-)
D. 0.1 mol / L 的硫酸铵溶液中:c(SO42-)>c(NH4+)> c(H+)> c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱性硼化钒(VB2)—空气电池工作时反应为:4VB2+11O2=4B2O3+2V2O5,用该电池电解100mL 硫酸铜溶液,实验装置如图所示(b、c均为惰性电极),当外电路中通过0.02mol电子时,B装置两极共收集到0.224L气体(标准状况)。下列说法正确的是( )
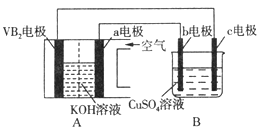
A. 电解过程中,b电极表面先有红色物质析出,然后有气泡产生
B. VB2为负极,电极反应为:2VB2+11H2O-22e-=V2O5+2B2O3+22H+
C. 电池内部OH-移向a电极,溶液pH保持增大
D. 忽略溶液体积变化,电解后B装置中溶液的pH为1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.5 L 1 mol/L FeCl3溶液与0.2 L 1 mol/L KCl溶液中的Cl-的物质的量浓度之比( )
A.5:2 B. 3:1 C.15:2 D. 1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:
2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ·mol-1
Na2O2(s)+CO2(g)=Na2CO3(s)+![]() O2(g) ΔH=-266 kJ·mol-1
O2(g) ΔH=-266 kJ·mol-1
根据以上热化学方程式判断,下列说法正确的是( )
A.CO的标准燃烧热为283 kJ
B.下图可表示由CO生成CO2的反应过程和能量关系
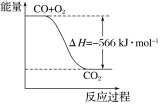
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ΔH>-532 kJ·mol-1
D.CO(g)与Na2O2(s)反应放出549 kJ热量时,电子转移数为6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质和对应用途的描述均正确的是
A. SiO2硬度大,可用于制造光导纤维
B. 碳具有还原性,可用碳在高温下将二氧化硅还原为硅
C. 铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸
D. 汽油是常见的有机溶剂,可以用裂化汽油来萃取溴水中的溴
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表述正确的是
A. 在食品袋中放入CaCl2·6H2O,可防止食物受潮
B. 硅是制造太阳能电池的常用材料
C. 四氧化三铁俗称铁红,可用作油漆、红色涂料
D. SO3溶于水形成的溶液能导电,所以SO3是电解质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com