
”¾ĢāÄæ”æÓŠ»śĪļ·Ö×ÓÖŠÓė”°O©C©”±ĻąĮ¬µÄĢ¼Ō×ÓÉĻµÄĒā»īŠŌ½Ļ“ó£¬æÉŅŌÓė¼×Č©»ņĀ±“śĢžµČ·¢Éś·“Ó¦£®ŅŃÖŖ£ŗ
ÓŠ»śĪļJŹĒÖŲŅŖµÄ¹¤ŅµŌĮĻ£¬ĘäŗĻ³ÉĀ·ĻßČēĻĀ£Ø²æ·Ö²śĪļŗĶ·“Ó¦Ģõ¼žĀŌ£©£ŗ
£Ø1£©AÖŠĖłŗ¬¹ŁÄÜĶŵÄĆū³ĘŹĒ £®
£Ø2£©A”śBµÄ·“Ó¦ĄąŠĶŹĒ·“Ó¦£®
£Ø3£©GĖ׳ĘĖõĘ»¹ūĖį£¬ÓėBŅŌĪļÖŹµÄĮæÖ®±Č1£ŗ2·“Ó¦£¬ŌņG+B”śHµÄ»Æѧ·½³ĢŹ½ŹĒ £®
£Ø4£©JµÄĶ¬·ÖŅģ¹¹ĢåXŹōÓŚ·¼Ļć×å»ÆŗĻĪļ£¬1mol XÓė×ćĮæNa»ņNaOH·“Ó¦Ź±µÄĪļÖŹµÄĮæÖ®±Č·Ö±šŹĒ1£ŗ4ŗĶ1£ŗ1£¬ĒŅ±½»·ÉĻÖ»ÓŠŅ»ÖÖŅ»ĀČ“śĪļ£®·ūŗĻÉĻŹöĢõ¼žµÄXÓŠÖÖ£¬Š“³öĘäÖŠČĪŅāŅ»ÖֵĽį¹¹¼ņŹ½£ŗ £®
£Ø5£©ŅŃÖŖEÖŠÖ»ÓŠŅ»ÖÖ¹ŁÄÜĶÅ£¬ĒŅŗĖ“Ź²ÕńĒāĘ×ĻŌŹ¾Ęä·Ö×ÓÖŠÓŠĮ½ÖÖ²»Ķ¬»Æѧ»·¾³µÄĒā£®ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£ØĢīŠņŗÅ£©£»EµÄ·Ö×ÓŹ½ŹĒ £® a£®EÓėB»„ĪŖĶ¬ĻµĪļ
b£®EÖŠŗ¬ÓŠµÄ¹ŁÄÜĶÅŹĒōĒ»ł
c£®FŌŚŅ»¶ØĢõ¼žĻĀŅ²æÉ×Ŗ»ÆĪŖE
d£®FÖŠŅ²ÓŠĮ½ÖÖ²»Ķ¬»Æѧ»·¾³µÄĒā
£Ø6£©JµÄ½į¹¹¼ņŹ½ŹĒ £®
”¾“š°ø”æ
£Ø1£©Č©»ł
£Ø2£©¼Ó³É·“Ó¦
£Ø3£©HOOCCH2COOH+2C2H5OH ![]() C2H5OOCCH2COOC2H5+2H2O
C2H5OOCCH2COOC2H5+2H2O
£Ø4£©2£»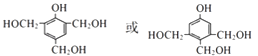
£Ø5£©bc£»C5H12O4
£Ø6£©![]()
”¾½āĪö”æ½ā£ŗAµÄ·Ö×ÓŹ½ĪŖC2H4O£¬ÓėHCHO·¢Éś·“Ó¦ŠÅĻ¢¢ŁµÄ·“Ó¦£¬ŌņAŗ¬ÓŠ©CHO£¬ŌņAĪŖCH3CHO£¬AÓėĒāĘų·¢Éś¼Ó³É·“Ӧɜ³ÉB£¬BĪŖCH3CH2OH£¬BÓėNa·“Ӧɜ³ÉCĪŖCH3CH2ONa£®GĖ׳ĘĖõĘ»¹ūĖį£¬ÓėŅŅ“¼ŅŌĪļÖŹµÄĮæÖ®±Č1£ŗ2·“Ó¦£¬ŌņGĪŖ¶žŌŖĖį£¬¹ŹGĪŖHOOCCH2COOH£¬ŌņHĪŖC2H5OOCCH2COOC2H5 £® ÓÉ×Ŗ»Æ¹ŲĻµæÉÖŖ£¬F”¢H·¢ÉśŠÅĻ¢·“Ó¦¢ŚÖŠµÄµŚŅ»²½·“Ӧɜ³ÉI£¬I·¢ÉśŠÅĻ¢·“Ó¦¢ŚÖŠµÄµŚ¶ž²½·“Ӧɜ³ÉJ£¬ŌņFĪŖäå“śĪļ£¬¹ŹDÓėĒāĘų·¢Éś¼Ó³É·“Ó¦·“Ӧɜ³ÉE£¬EŌŁÓėHBr·¢ÉśČ”“ś·“Ӧɜ³ÉF£¬EÖŠÖ»ÓŠŅ»ÖÖ¹ŁÄÜĶÅ£¬ŌņEÖŠŗ¬ÓŠ¹ŁÄÜĶÅĪŖ©OH£¬ĒŅEŗĖ“Ź²ÕńĒāĘ×ĻŌŹ¾Ęä·Ö×ÓÖŠÓŠĮ½ÖÖ²»Ķ¬»Æѧ»·¾³µÄĒā£¬ÓÉ·“Ó¦ŠÅĻ¢¢ŁæÉÖŖ»į²śÉś»łĶÅ©CH2OH£¬øĆ»łĶÅŗ¬ÓŠ2ÖÖ²»Ķ¬HŌ×Ó£¬ĒŅ©CHO»¹Ō±äĪŖ©CH2OH£¬¹ŹEĪŖC£ØCH2OH£©4 £¬ FĪŖC£ØCH2Br£©4 £¬ 3·Ö×ÓHCHOÓė1·Ö×ÓCH3CHO·¢Éś¼Ó³É·“Ӧɜ³ÉD£¬DĪŖ£ØHOCH2£©3CCHO£®F”¢H·¢ÉśŠÅĻ¢·“Ó¦¢ŚÖŠµÄµŚŅ»²½·“Ӧɜ³ÉI£¬IĪŖ ![]() £¬I·¢ÉśŠÅĻ¢·“Ó¦¢ŚÖŠµÄµŚ¶ž²½·“Ӧɜ³ÉJ£¬JĪŖ
£¬I·¢ÉśŠÅĻ¢·“Ó¦¢ŚÖŠµÄµŚ¶ž²½·“Ӧɜ³ÉJ£¬JĪŖ ![]() £¬£Ø1£©AĪŖCH3CHO£¬Ėłŗ¬¹ŁÄÜĶŵÄĆū³ĘŹĒ£ŗČ©»ł£»ĖłŅŌ“š°øŹĒ£ŗČ©»ł£»£Ø2£©A”śBŹĒCH3CHOÓėĒāĘų·¢Éś¼Ó³É·“Ӧɜ³ÉCH3CH2OH£¬ ĖłŅŌ“š°øŹĒ£ŗ¼Ó³É·“Ó¦£»£Ø3£©GĖ׳ĘĖõĘ»¹ūĖį£¬ÓėBŅŌĪļÖŹµÄĮæÖ®±Č1£ŗ2·“Ó¦£¬G+B”śHµÄ»Æѧ·½³ĢŹ½ŹĒ£ŗHOOCCH2COOH+2C2H5OH
£¬£Ø1£©AĪŖCH3CHO£¬Ėłŗ¬¹ŁÄÜĶŵÄĆū³ĘŹĒ£ŗČ©»ł£»ĖłŅŌ“š°øŹĒ£ŗČ©»ł£»£Ø2£©A”śBŹĒCH3CHOÓėĒāĘų·¢Éś¼Ó³É·“Ӧɜ³ÉCH3CH2OH£¬ ĖłŅŌ“š°øŹĒ£ŗ¼Ó³É·“Ó¦£»£Ø3£©GĖ׳ĘĖõĘ»¹ūĖį£¬ÓėBŅŌĪļÖŹµÄĮæÖ®±Č1£ŗ2·“Ó¦£¬G+B”śHµÄ»Æѧ·½³ĢŹ½ŹĒ£ŗHOOCCH2COOH+2C2H5OH ![]() C2H5OOCCH2COOC2H5+2H2O£¬
C2H5OOCCH2COOC2H5+2H2O£¬
ĖłŅŌ“š°øŹĒ£ŗHOOCCH2COOH+2C2H5OH ![]() C2H5OOCCH2COOC2H5+2H2O£»£Ø4£©
C2H5OOCCH2COOC2H5+2H2O£»£Ø4£© ![]() µÄĶ¬·ÖŅģ¹¹ĢåXŹōÓŚ·¼Ļć×å»ÆŗĻĪļ£¬ŗ¬ÓŠ1øö±½»·£¬1molXÓė×ćĮæNa»ņNaOH·“Ó¦Ź±µÄĪļÖŹµÄĮæÖ®±Č·Ö±šŹĒ1£ŗ4ŗĶ1£ŗ1£¬ŌņXŗ¬ÓŠ4øö©OH£¬ĘäÖŠ1øöĪŖ·ÓōĒ»ł£¬ĒŅ±½»·ÉĻÖ»ÓŠŅ»ÖÖŅ»ĀČ“śĪļ£¬·ūŗĻÉĻŹöĢõ¼žµÄX½į¹¹¼ņŹ½ÓŠ£ŗ
µÄĶ¬·ÖŅģ¹¹ĢåXŹōÓŚ·¼Ļć×å»ÆŗĻĪļ£¬ŗ¬ÓŠ1øö±½»·£¬1molXÓė×ćĮæNa»ņNaOH·“Ó¦Ź±µÄĪļÖŹµÄĮæÖ®±Č·Ö±šŹĒ1£ŗ4ŗĶ1£ŗ1£¬ŌņXŗ¬ÓŠ4øö©OH£¬ĘäÖŠ1øöĪŖ·ÓōĒ»ł£¬ĒŅ±½»·ÉĻÖ»ÓŠŅ»ÖÖŅ»ĀČ“śĪļ£¬·ūŗĻÉĻŹöĢõ¼žµÄX½į¹¹¼ņŹ½ÓŠ£ŗ 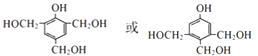 £¬¹²ÓŠĮ½ÖÖ£¬ĖłŅŌ“š°øŹĒ£ŗ2£»
£¬¹²ÓŠĮ½ÖÖ£¬ĖłŅŌ“š°øŹĒ£ŗ2£» 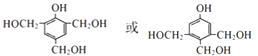 £»£Ø5£©a£®EĪŖC£ØCH2OH£©4 £¬ BĪŖCH3CH2OH£¬EÓėBŗ¬ÓŠōĒ»łŹżÄæ²»Ķ¬£¬²»ŹĒĶ¬ĻµĪļ£¬¹Źa“ķĪó£»b£®EĪŖC£ØCH2OH£©4 £¬ ŗ¬ÓŠµÄ¹ŁÄÜĶÅŹĒōĒ»ł£¬¹ŹbÕżČ·£»c£®FĪŖC£ØCH2Br£©£¬ŌŚĒāŃõ»ÆÄĘĖ®ČÜŅŗ”¢¼ÓČČĢõ¼žĻĀ·¢ÉśĖ®½ā·“Ó¦æÉ×Ŗ»ÆĪŖE£¬¹ŹcÕżČ·£»d£®FĪŖC£ØCH2Br£©£¬·Ö×ÓÖŠÖ»ÓŠ1ÖÖĒāŌ×Ó£¬¹Źd“ķĪó£»EĪŖC£ØCH2OH£©4 £¬ ·Ö×ÓŹ½ĪŖC5H12O4 £¬ ĖłŅŌ“š°øŹĒ£ŗbc£»C5H12O4£»£Ø6£©ÓÉÉĻŹö·ÖĪöæÉÖŖ£¬JµÄ½į¹¹¼ņŹ½ŹĒ
£»£Ø5£©a£®EĪŖC£ØCH2OH£©4 £¬ BĪŖCH3CH2OH£¬EÓėBŗ¬ÓŠōĒ»łŹżÄæ²»Ķ¬£¬²»ŹĒĶ¬ĻµĪļ£¬¹Źa“ķĪó£»b£®EĪŖC£ØCH2OH£©4 £¬ ŗ¬ÓŠµÄ¹ŁÄÜĶÅŹĒōĒ»ł£¬¹ŹbÕżČ·£»c£®FĪŖC£ØCH2Br£©£¬ŌŚĒāŃõ»ÆÄĘĖ®ČÜŅŗ”¢¼ÓČČĢõ¼žĻĀ·¢ÉśĖ®½ā·“Ó¦æÉ×Ŗ»ÆĪŖE£¬¹ŹcÕżČ·£»d£®FĪŖC£ØCH2Br£©£¬·Ö×ÓÖŠÖ»ÓŠ1ÖÖĒāŌ×Ó£¬¹Źd“ķĪó£»EĪŖC£ØCH2OH£©4 £¬ ·Ö×ÓŹ½ĪŖC5H12O4 £¬ ĖłŅŌ“š°øŹĒ£ŗbc£»C5H12O4£»£Ø6£©ÓÉÉĻŹö·ÖĪöæÉÖŖ£¬JµÄ½į¹¹¼ņŹ½ŹĒ ![]() £¬ĖłŅŌ“š°øŹĒ£ŗ
£¬ĖłŅŌ“š°øŹĒ£ŗ ![]() £®
£®


 ½Ģ²ÄČ«½ā×Ö“Ź¾äĘŖĻµĮŠ“š°ø
½Ģ²ÄČ«½ā×Ö“Ź¾äĘŖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
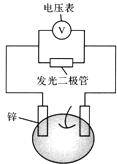
”¾ĢāÄæ”æĮōŠÄ“¦“¦½ŌѧĪŹ£®“ÓÉś»ī³ö·¢½ųŠŠæĘѧĢ½¾æ£¬æÉŅŌ»ńµĆ×ŌŠÅ£¬ŠĪ³ÉÕżČ·µÄĖ¼Ī¬·½Ź½£®¼×”¢ŅŅĮ½Ī»Ķ¬Ń§Ņ»ĘšŗĻ×÷Éč¼ĘĶź³ÉĮĖĖ®¹ūµē³ŲµÄŹµŃé£ØČēĶ¼£©£¬²āµĆŹż¾ŻČēĻĀ
ŹµŃéŠņŗÅ | µē¼«²ÄĮĻ | Ė®¹ūÖÖĄą | µē¼«¼ä¾ąĄė/cm | µēŃ¹/mV |
1 | ŠæĶ | ²¤ĀÜ | 3 | 900 |
2 | ŠæĶ | Ę»¹ū | 3 | 650 |
3 | ŠæĶ | øĢéŁ | 3 | 850 |
4 | ŠæĶ | Ī÷ŗģŹĮ | 3 | 750 |
5 | ŠæĀĮ | ²¤ĀÜ | 3 | 650 |
6 | ŠæĀĮ | Ę»¹ū | 3 | 450 |
¶Ō¼×Ķ¬Ń§Ģį³öµÄĪŹĢā£¬ŅŅĶ¬Ń§µÄ½āŹĶ²»ÕżČ·µÄŹĒ£Ø £©
¼×Ķ¬Ń§ | ŅŅĶ¬Ń§ | |
A | ŹµŃé6ÖŠøŗ¼«µē¼«·“Ó¦Ź½ČēŗĪŠ“£æ | Al©3e©=Al3+ |
B | ŹµŃé1£¬5ÖŠµēĮ÷·½ĻņĪŖŹ²Ć“Ļą·“£æ | 1ÖŠŠæĪŖøŗ¼«£¬µēĮ÷ÓÉĶ¾µ¼ĻßĮ÷ĻņŠæ£¬5ÖŠĀĮĪŖøŗ¼«£¬ĀĮŹ§Č„µē×Ó£¬µēĮ÷ÓÉŠæ¾µ¼ĻßĮ÷ĻņĀĮ |
C | Ė®¹ūµē³ŲµÄµēŃ¹ÓėÄÄŠ©ŅņĖŲÓŠ¹Ų£æ | Ö»øśĖ®¹ūµÄĄąŠĶÓŠ¹Ų |
D | ŹµŃéÖŠ·¢¹ā¶ž¼«¹Ü²»ĮĮ£¬ČēŗĪŹ¹ĖüĮĮĘšĄ“ | æÉÓĆĶŠæ×÷µē¼«£¬ÓĆ²¤ĀÜ×÷½éÖŹ£¬²¢½«¶ąøö“Ėµē³Ų“®ĮŖĘšĄ“ |
A.A
B.B
C.C
D.D
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖĪĀ¶ČTŹ±£¬Ė®µÄĄė×Ó»ż³£ŹżĪŖKw£¬øĆĪĀ¶ČĻĀ£¬½«ÅضČĪŖa molL©1µÄŅ»ŌŖĖįHAČÜŅŗÓėb molL©1µÄŅ»ŌŖ¼īBOHČÜŅŗµČĢå»ż»ģŗĻ£¬æÉÅŠ¶ĻøĆČÜŅŗŅ»¶Ø³ŹÖŠŠŌµÄŅĄ¾ŻŹĒ£Ø £©
A.»ģŗĻČÜŅŗµÄPH=7
B.»ģŗĻČÜŅŗÖŠ£¬C£ØH+£©= ![]() mol?L©1
mol?L©1
C.a=b
D.»ģŗĻČÜŅŗÖŠ£¬C£ØH+£©+C£ØB+£©=C£ØOH©£©+C£ØA©£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¹ĢĢ¬»ÆŗĻĪļAÓÉĮ½ÖÖ¶ĢÖÜĘŚŌŖĖŲ×é³É£¬æÉÓėĖ®·¢Éśø“·Ö½ā·“Ó¦£®¼××éĶ¬Ń§ÓĆČēĶ¼×°ÖĆ£Ø¼Š³Ö×°ÖĆĀŌ£©¶ŌĘä½ųŠŠĢ½¾æŹµŃ飮
£Ø1£©ŅĒĘ÷BµÄĆū³ĘŹĒ £®
£Ø2£©ŹµŃéÖŠ£¬¢ņÖŠµÄŹŌÖ½±äĄ¶£¬¢ōÖŠŗŚÉ«·ŪÄ©Öš½„±äĪŖŗģÉ«£¬²¢ÓŠMÉś³É£¬Ōņ¢óÖŠµÄŹŌ¼ĮĪŖ £¬ ¢ōÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ £¬ ¢õÖŠµÄŹŌ¼ĮĪŖ £®
£Ø3£©ŅŅ×éĶ¬Ń§½ųŠŠĶ¬ŃłŹµŃ飬µ«×°ÖĆĮ¬½ÓĖ³ŠņĪŖ¢ń©¢ó©¢ō©¢ņ©¢õ©¢ö£¬“ĖŹ±¢ņÖŠĻÖĻóĪŖ £¬ ŌŅņŹĒ £®
£Ø4£©¾ÉĻŹö·“Ó¦£¬2.5g»ÆŗĻĪļAĄķĀŪÉĻæɵƵ½0.56L£Ø±ź×¼×“æö£©M£¬ŌņAµÄ»ÆѧŹ½ĪŖ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĻ©ĢžĒā»ÆŗóµĆµ½µÄ±„ŗĶĢžŹĒ ![]() £¬ŌņŌĻ©ĢžæÉÄÜÓŠµÄ½į¹¹¼ņŹ½ÓŠ£Ø £©
£¬ŌņŌĻ©ĢžæÉÄÜÓŠµÄ½į¹¹¼ņŹ½ÓŠ£Ø £©
A.1ÖÖ
B.2ÖÖ
C.3ÖÖ
D.4ÖÖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĄė×Ó·½³ĢŹ½ŹéŠ“ÕżČ·µÄŹĒ
A. Ģ¼ĖįÄĘČÜŅŗÖŠµĪČė¹żĮæµÄ“×ĖįČÜŅŗ£ŗCO32££«2H£«=H2O£«CO2
B. Fe3+µÄ¼ģŃé£ŗFe3£«£«3SCN£![]() Fe(SCN)3”ż
Fe(SCN)3”ż
C. ĖįŠŌČÜŅŗÖŠKIO3ÓėKI·“Ӧɜ³ÉI2£ŗIO3©+5I©+6H+=3I2+3H2O
D. Ģ¼ĖįĒāøĘČÜŅŗÖŠ¼ÓČė¹żĮæµÄĒāŃõ»ÆÄĘČÜŅŗ£ŗCa2£«£«HCO3££«OH£=CaCO3£«H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ25”ę£¬101kPaĢõ¼žĻĀ£¬½«15L O2ĶØČė10LCOŗĶH2µÄ»ģŗĻĘųÖŠ£¬Ź¹ĘäĶźČ«Č¼ÉÕ£¬øÉŌļŗ󣬻Öø“ÖĮŌĄ“µÄĪĀ¶ČŗĶŃ¹Ē森
£Ø1£©ČōŹ£ÓąĘųĢåµÄĢå»żŹĒ15L£¬ŌņŌCOŗĶH2µÄ»ģŗĻĘųÖŠV£ØCO£©=L£¬V£ØH2£©=L£®
£Ø2£©ČōŹ£ÓąĘųĢåµÄĢå»żĪŖa L£¬ŌņŌCOŗĶH2µÄ»ģŗĻĘųÖŠV£ØCO£©£ŗV£ØH2£©= £®
£Ø3£©ČōŹ£ÓąĘųĢåµÄĢå»żĪŖaL£¬ŌņaµÄȔֵ·¶Ī§ŹĒ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻņmgĆ¾ŗĶĀĮµÄ»ģŗĻĪļÖŲ¼ÓČėŹŹĮæµÄĻ”ĮņĖį£¬Ē”ŗĆĶźČ«·“Ӧɜ³É±ź×¼×“æöĻĀµÄĘųĢåbL£®Ļņ·“Ó¦ŗóµÄČÜŅŗÖŠ¼ÓČėcmol/LĒāŃõ»Æ¼ŲČÜŅŗVmL£¬Ź¹½šŹōĄė×ÓøÕŗĆ³ĮµķĶźČ«£¬µĆµ½µÄ³ĮµķÖŹĮæĪŖng£®ŌŁ½«µĆµ½µÄ³Įµķ×ĘÉÕÖĮÖŹĮæ²»ŌŁøıäĪŖÖ¹£¬µĆµ½¹ĢĢåpg£®ŌņĻĀĮŠ¹ŲĻµ²»ÕżČ·µÄŹĒ£Ø £©
A.c= ![]()
B.p=m+ ![]()
C.n=m+17Vc
D.![]() m£¼p£¼
m£¼p£¼ ![]() m
m
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹ŲÓƶčŠŌµē¼«µē½āAgNO3ČÜŅŗµÄĖµ·Ø²»ÕżČ·µÄŹĒ(””””)
A.µē½ā¹ż³ĢÖŠŅõ¼«ÖŹĮæ²»¶ĻŌö“ó
B.µē½ā¹ż³ĢÖŠŃō¼«ø½½üµÄpH²»¶Ļ½µµĶ
C.µē½āŅ»¶ĪŹ±¼äŗó£¬ĻņČÜŅŗÖŠ¼ÓČėŹŹĮæµÄAg2O¹ĢĢåæÉŹ¹ČÜŅŗ»Öø“µ½µē½āĒ°µÄדæö
D.µē½ā¹ż³ĢÖŠ£¬ČÜŅŗÖŠµē×ÓÓÉŅõ¼«ĒØĻņŃō¼«
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com