
| ʵ����� | �� | �� | �� |
| �Ͻ�����/g | 8.8 | 17.6 | 22.0 |
| �������/L | 2.24 | 4.48 | 4.48 |
���� ��1���ٸ���n=$\frac{V}{{V}_{m}}$�������״����33.6L�����������ʵ�����
�����CO��CO2�����ʵ������ֱ�������ʵ�����������ʽ���㣻
��2�����ݱ����ݿ�֪������8.8g�Ͻ�����2.24L����������17.6g�Ͻ�����4.48L�������Ҹ��ݱ���֪�ټ���Ͻ�ʱ������������䣬˵�����������������������ǡ�÷�Ӧ�����кϽ������������ȫ��Ӧ���ݴ˽��н��
��� �⣺��1�����ڱ�״���£�CO��CO2�Ļ�����干33.6L��������������ʵ���Ϊ��$\frac{33.6L}{22.4L/mol}$=1.5mol��
�ʴ�Ϊ��1.5 mol��
������������CO��CO2�����ʵ����ֱ�Ϊx��y��
��$\left\{\begin{array}{l}{28x+44y=50}\\{x+y=1.5}\end{array}\right.$
��ã�$\left\{\begin{array}{l}{x=1mol}\\{y=0.5mol}\end{array}\right.$
ԭ�Ӹ���֮�ȵ��������ʵ���֮�ȣ���C��Oԭ�Ӹ�����=��1mol+0.5mol������1mol+0.5mol��2��=3��4��
�ʴ�Ϊ��3��4��
��2���ټ���8.8g�Ͻ�����2.24L����������17.6g�Ͻ�����4.48L�������Ҹ��ݱ���֪�ټ���Ͻ�ʱ������������䣬˵�����������������������ǡ�÷�Ӧ�����кϽ������������ȫ��Ӧ��
A������ʵ���ҺϽ��������ӣ������������������˵��ʵ����кϽ��㣬����û����ȫ��Ӧ����A����
B�����ݱ������ݿ�֪����������������Ϊ4.48L���ҽ�ϼ�֪����4.48L�������ĺϽ�����Ϊ17.6g��˵��ʵ�����н���þ������ǡ����ȫ��Ӧ����B��ȷ��
C�����кϽ�����������ʵ�����ʣ�������������ᣬ������������������C��ȷ��
D��ͭ�����Խ������������ᷴӦ����D����
�ʴ�Ϊ��BC��
�ڸ����ҡ�����֪��100mL��������ȫ��Ӧ������ɱ�״�����������Ϊ4.48L����100mL�������к���HCl�����ʵ���Ϊ��n��HCl��=2n��H2��=$\frac{4.48L}{22.4L/mol}$��2=0.4mol���������Ũ��Ϊ��$\frac{0.4mol}{0.1L}$=4mol/L��
���кϽ���ȫ��Ӧ���������������ʵ���Ϊ��$\frac{2.24L}{22.4L/mol}$=0.1mol��ͭ�������ᷴӦ����8.8g�Ͻ��к���Mg�����ʵ���Ϊ0.1mol������Ϊ��24g/mol��0.1mol=2.4g��
���ԸúϽ���Mg����������Ϊ��$\frac{2.4g}{8.8g}$��100%=27.3%��
�ʴ�Ϊ��4mol•L-1��27.3%��
���� ���⿼���˻���ﷴӦ�ļ��㡢���ʵ���Ũ�ȵļ��㣬��Ŀ�Ѷ��еȣ���ȷ���ʵ���������Ħ�������Ħ������������٤������֮��Ĺ�ϵΪ���ؼ�����2��Ϊ�ѵ㡢�״��㣬ע����ȷ�жϷ�Ӧ�����������������������ѧ���ķ�����������������ѧ����������


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʵ����ʣ��ҩƷӦ�Ż�ԭ�Լ�ƿ�� | |
| B�� | �и����ʱӦ����ˮ�½��� | |
| C�� | ��ij������Һ��pHʱ������ˮ��pH��ֽʪ�� | |
| D�� | �ڡ����������������ʵ�ȥ����ʵ���У����������е���Һֱ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �û��ξ��к�Ư�����ƵĻ�ѧ���� | |
| B�� | �û��ε�ˮ��Һ������ | |
| C�� | �û��������ᷴӦ����1Ħ������ʱ��ת����1Ħ������ | |
| D�� | �û�������Ԫ�صĻ��ϼ�Ϊ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ͨˮ��Ͳ�������Ҫԭ�϶��õ�ʯ��ʯ | |
| B�� | ��ҵ���Ʋ�������������������ŷ� | |
| C�� | �������ǽ�������ά�߷��Ӳ��ϸ��϶��ɵĸ��ϲ��� | |
| D�� | ���й�����Ӣ�ĵ��ʽ�China�����������й������ij�����ʳ������磬�����������մ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ʯ��ʯī | B�� | ���ͺ��� | C�� | Na2O��Na2O2 | D�� | �����ͳ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
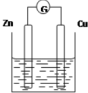 ��ͼ����Zn��CuΪ�缫��ϡH2SO4Ϊ�������Һ�γɵ�ԭ��أ�ijʵ����ȤС������ʵ����ڶ��鿨Ƭ�ϼ�¼���£�
��ͼ����Zn��CuΪ�缫��ϡH2SO4Ϊ�������Һ�γɵ�ԭ��أ�ijʵ����ȤС������ʵ����ڶ��鿨Ƭ�ϼ�¼���£��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com