
配制400 mL 0.5 mol·L-1的NaOH溶液,试回答下列问题:
(1)计算:需要NaOH固体的质量为______。
(2)某学生用托盘天平称量一个小烧杯的质量,称量前把游码放在标尺的零刻度处,天平静止时发现 指针在分度盘的偏右位置,此时左边的托盘将______(填“高于”或“低于”)右边的托盘。欲使天平平衡,所进行的操作为_______。假定最终称得小烧杯的质量为______(填“32.6 g”或“31.61 g”),
(3)配制方法:设计五个操作步骤:
① 向盛有NaOH的烧杯中加入200 mL蒸馏水使其溶解,并冷却至室温;
② 继续往容量瓶中加蒸馏水至液面接近刻度线1~2 cm处;
③ 将NaOH溶液沿玻璃棒注入500 mL容量瓶中;
④ 在烧杯中加入少量的蒸馏水,小心洗涤2~3次后移入容量瓶;
⑤ 改用胶头滴管加蒸馏水至刻度线,加盖摇匀。
试将以上操作排出先后顺序______。
(4)某学生实际配制NaOH溶液的浓度为0.48 mol·L-1,原因可能是______。
A.使用滤纸称量氢氧化钠固体
B.容量瓶中原来存有少量蒸馏水
C.溶解NaOH的烧杯未经多次洗涤
D.胶头滴管加水后定容时仰视刻度
(5)在下列配制0.5 mol·L-1 NaOH溶液过程示意图中有错误的是(填序号)______。
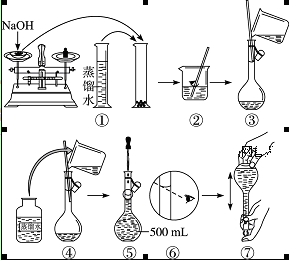
(1)10.0 g (2)高于 将左边的平衡螺母左旋移动(或将右边的平衡螺母左旋),直至天平平衡 32.6 g(每空1分)(3)① ③ ④ ② ⑤ (4)ACD (5)① ③ ⑥ (每空2分)
【解析】
试题分析:(1) 因为没有400ml的容量瓶,所以配置400mL 0.5 mol·L-1的NaOH溶液,要用500ml的容量瓶,计算时溶液的体积应以500ml为标准,因此,n(NaOH)=0.5L×0.5 mol·L-1=0.25mol,则氢氧化钠的质量为:0.25mol×40g/mol=10.0 g(2) 天平静止时发现指针在分度盘的偏右位置,说明天平右端重,所以, 可采取将左边的平衡螺母左旋移动(或将右边的平衡螺母左旋),直至天平平衡,由于天平的精确度是0.1g,所以最终称得小烧杯的质量为可选32.6 g;(3)按照一定物质的量浓度的溶液的配置步骤应为① ③ ④ ② ⑤ ;⑷A、氢氧化钠有吸水性,在滤纸上发生潮解,从而使氢氧化钠的量减少,致使浓度降低,正确;B、容量瓶中配制溶液本来就是一个加水不断稀释的过程,原来有水不受影响,错误;C、溶解NaOH的烧杯未经多次洗涤会造成进入容量中的溶质减少,正确;D、胶头滴管加水后定容时仰视刻度,会造成加水量增多,从而使氢氧化钠的浓度降低。因此正确选应为ACD。(5)不能将固体氢氧化钠放入到量筒中,用玻璃棒引流时要将玻璃棒插入到容量瓶瓶颈刻度线的下方,读数时要平时,答案:① ③ ⑥
考点:考查一定物质的量浓度的溶液的配置步骤、误差分析及化学实验操作。


科目:高中化学 来源: 题型:
8![]() +5Cu2S+44H+====10Cu2++5SO2+8Mn2++22H2O
+5Cu2S+44H+====10Cu2++5SO2+8Mn2++22H2O
6![]() +5CuS+28H+====5Cu2++5SO2+6Mn2++14H2O
+5CuS+28H+====5Cu2++5SO2+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350 mL 0.1 mol·L-1 (NH4)2Fe(SO4)2溶液完全反应。
(1)配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:
___![]() +_____Fe2++______H+====______Mn2++______Fe3++______H2O
+_____Fe2++______H+====______Mn2++______Fe3++______H2O
(2)KMnO4溶液与混合物反应后,剩余KMnO4的物质的量为_________ mol。
(3)欲配制500 mL 0.1 mol·L-1 Fe2+溶液,需称取(NH4)2Fe(SO4)2?·6H2O(M=
(4)混合物中Cu2S的质量分数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
2 g Cu2S和CuS的混合物在酸性溶液中用400 mL 0.075 mol·L-1 KMnO4溶液处理,发生反应如下:
![]() 8
8![]() +5Cu2S+44H+====10Cu2++5SO2+8Mn2++22H2O
+5Cu2S+44H+====10Cu2++5SO2+8Mn2++22H2O
![]() 6
6![]() +5CuS+28H+====5Cu2++5SO2+6Mn2++14H2O
+5CuS+28H+====5Cu2++5SO2+6Mn2++14H2O
![]() 反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350 mL 0.1 mol·L-1(NH4)2Fe(SO4)2溶液完全反应。
反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350 mL 0.1 mol·L-1(NH4)2Fe(SO4)2溶液完全反应。![]()

![]()
![]()
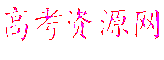
![]() (1)配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:
(1)配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:
![]()
![]()
![]() +
+![]() Fe2++
Fe2++![]() H+
H+![]() Mn2++
Mn2++![]() Fe3++
Fe3++![]() H2O
H2O
![]() (2)KMnO4溶液与混合物反应后,剩余KMnO4的物质的量为_________mol。
(2)KMnO4溶液与混合物反应后,剩余KMnO4的物质的量为_________mol。
![]() (3)欲配制500 mL 0.1 mol·L-1 Fe2+溶液,需称取(NH4)2Fe(SO4)2·6H2O(M=392 g·mol-1)的质量为_________ g。
(3)欲配制500 mL 0.1 mol·L-1 Fe2+溶液,需称取(NH4)2Fe(SO4)2·6H2O(M=392 g·mol-1)的质量为_________ g。
![]() (4)混合物中Cu2S的质量分数为_________。
(4)混合物中Cu2S的质量分数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(10分)2 g Cu2S和CuS的混合物在酸性溶液中用400 mL 0.075 mol·L-1 KMnO4溶液处理,发生反应如下:
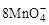 +5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
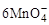 +5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350 mL 0.1 mol·L-1(NH4)2Fe(SO4)2溶液完全反应。
(1)配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:
______![]() +______Fe2++______H+=______Mn2++______Fe3++______H2O
+______Fe2++______H+=______Mn2++______Fe3++______H2O
(2)KMnO4溶液与混合物反应后,剩余KMnO4的物质的量为________mol。
(3)欲配制500 mL0.1 mol·L-1 Fe2+溶液,需称取(NH4)2Fe(SO4)2·6H2O(M=392 g·mol-1)的质量为________g。
(4)混合物中Cu2S的质量分数为_______。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年高三上学期化学《晶体、化学反应中的物质和能量变化》单元测试卷(1) 题型:计算题
(10分)2 g Cu2S和CuS的混合物在酸性溶液中用400 mL 0.075 mol·L-1 KMnO4溶液处理,发生反应如下:
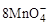 +5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
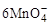 +5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350 mL 0.1 mol·L-1(NH4)2Fe(SO4)2溶液完全反应。
(1)配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:
______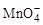 +______Fe2++______H+=______Mn2++______Fe3++______H2O
+______Fe2++______H+=______Mn2++______Fe3++______H2O
(2)KMnO4溶液与混合物反应后,剩余KMnO4的物质的量为________mol。
(3)欲配制500 mL 0.1 mol·L-1 Fe2+溶液,需称取(NH4)2Fe(SO4)2·6H2O(M=392 g·mol-1)的质量为________g。
(4)混合物中Cu2S的质量分数为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com