
| A. | 11.7mol/L | B. | 12.7mol/L | C. | 13.7mol/L | D. | 14.7mol/L |
分析 标况下,n(HCl)=$\frac{448L}{22.4L/mol}$=20mol,m(HCl)=20mol×36.5g/mol=73g,水的质量为1000g,溶液的质量分数为$\frac{730g}{730g+1000g}$=0.4219,再根据C=$\frac{1000ρw}{M}$计算盐酸的物质的量浓度.
解答 解:标况下,n(HCl)=$\frac{448L}{22.4L/mol}$=20mol,m(HCl)=20mol×36.5g/mol=73g,水的质量为1000g,溶液的质量分数为$\frac{730g}{730g+1000g}$=0.4219,所以溶液中氯化氢的浓度C=$\frac{1000ρw}{M}$=$\frac{1000×1.1×0.4219}{36.5}$=12.7mol/L,
故选:B.
点评 本题考查物质的量浓度计算,根据公式C=$\frac{1000ρw}{M}$分析解答即可,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:实验题
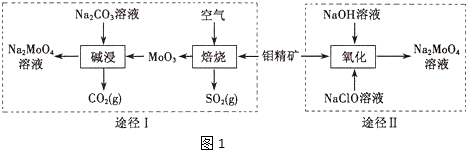
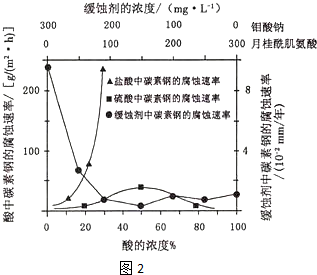
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
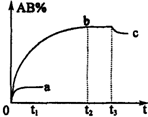 反应A2+B2?2AB;△H=Q,在不同温度和压强改变的条件下,产物AB的质量分数AB%生成情况如图:a为500℃时的情况;b为300℃时的情况;c为反应在300℃时从时间t3开始向容器中加压的情况.则下列叙述正确的是( )
反应A2+B2?2AB;△H=Q,在不同温度和压强改变的条件下,产物AB的质量分数AB%生成情况如图:a为500℃时的情况;b为300℃时的情况;c为反应在300℃时从时间t3开始向容器中加压的情况.则下列叙述正确的是( )| A. | A2、B2及AB均为气体,Q>0 | |
| B. | AB为气体,A2、B2中至少有一种为非气体,Q<0 | |
| C. | AB为气体,A2、B2中有一种为气体,Q<0 | |
| D. | AB为固体,A2、B2中有一种为非气体,Q>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将pH=11的氢氧化钠溶液加水稀释100倍,溶液中c(H+)=10-13 mol•L-1 | |
| B. | 将pH=9的氢氧化钠溶液和pH=13的氢氧化钡溶液等体积混合,所得混合溶液的pH=11 | |
| C. | 将pH=13的氢氧化钡溶液和pH=1的盐酸等体积混合,由于氢氧化钡过量,所得溶液的pH>7 | |
| D. | 将pH=1的硫酸和pH=5的盐酸等体积混合,所得混合溶液的pH=1.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体不均一、不稳定,静置后易产生沉淀,溶液均一、稳定、静置不产生沉淀 | |
| B. | 溶液和胶体都是纯净物,浊液是混合物 | |
| C. | 光线通过时,胶体产生丁达尔效应,溶液则无丁达尔效应 | |
| D. | 只有胶状物如胶水、果冻类的物质才能称为胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酒精受热变为气体 | B. | 氯化铵受热变为气体 | ||
| C. | 二氧化硅受热熔化 | D. | 食盐溶解在水中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com