
氨气是重要的化工原料。
38.1.实验室可用浓氨水和_____(选填编号)来制取氨气。
a.烧碱 b.生石灰 c.氯化铵
检验氨气易溶于水的简单操作是:收集一试管氨气, 。
39.2.往饱和食盐水中依次通入足量的NH3和足量的CO2,生成沉淀的化学式为 ;过滤后,使余液尽可能析出较多NH4Cl晶体的方法是:再通入足量的NH3、冷却并加入 。
侯德榜制碱法(联合氨碱法)的CO2来自_____(选填编号)。
a.石灰石煅烧 b.含碳物质燃烧 c.合成氨厂的副产品
40.3.往CuSO4溶液中滴加氨水,先有沉淀析出,后沉淀溶解溶液呈深(绛)蓝色,有[Cu(NH3)4]2+生成。往溶液中滴加稀硫酸,溶液变为淡蓝色。颜色变浅的主要原因可能是:
①溶液变稀;
② [Cu(NH3)4]2++4H+ Cu2+ + 4NH4+
Cu2+ + 4NH4+
请设计一个简单实验说明溶液变浅的主要原因 。
41.4.某实验小组设计了下列装置进行氨的催化氧化实验。
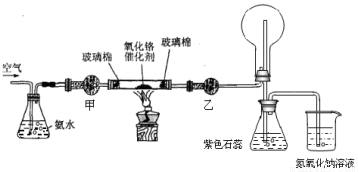
(1)实验时发现:如果缺少乙处的干燥管,将反应后的气体直接通入烧瓶,则烧瓶中先产生白雾,随即产生白烟,其原因可用化学方程式表示为: 、 。
(2)实验前,烧杯中盛有200mL 1.000 mol/L NaOH溶液,实验后将烧杯中溶液蒸干,再将所得固体加热至恒重,得到固体10.9g,则该固体含NaOH g。
38.1.ab;倒插入水中,水迅速充满试管;
39.2.NaHCO3;NaCl;c;
40.3.往深蓝色溶液中通入少量HCl气体或氨气或滴加浓硫酸或加少量NaOH固体或将稀溶液蒸发(合理即可);
41.4.(1) 4NO+3O2+2H2O 4HNO3(合理即可)、NH3+HNO3→NH4NO3;
4HNO3(合理即可)、NH3+HNO3→NH4NO3;
(2)4。
【解析】
试题分析:38.1.浓氨水中存在以下平衡过程:
NH3+H2ONH3·H2ONH4++OH-
加入烧碱溶于水放热、c(OH-)增大,平衡左移,放出氨气,故可以用来制取氨气。
加入生石灰与水反应放热、生成Ca(OH)2,c(OH-)增大,平衡左移,放出氨气,故可以用来制取氨气。检验氨气易溶于水的简单操作是:收集一试管氨气,倒插入水中,水迅速充满试管。
39.2.往饱和食盐水中依次通入足量的NH3和足量的CO2,
NaCl+CO2+NH3+H2O=NH4Cl+NaHCO3↓
生成沉淀的化学式为NaHCO3;
过滤后,再通入足量的NH3、冷却并加入NaCl,由于溶液中有大量的NH4+、Cl-低温下NH4Cl的溶解度降低,则可析出较多NH4Cl;
侯德榜制碱法是以食盐、氨及合成氨工业副产的二氧化碳为原料,同时生产纯碱及氯化铵,即联合产纯碱与氯化铵,故c正确。
40.3.将稀溶液蒸发观察是否变深用来确定是否是可能①,往深蓝色溶液中通入少量HCl气体或氨气或滴加浓硫酸或加少量NaOH固体若确定是否是可能②。
41.4.4】(1)由装置流程可知:缺少乙处的干燥管,NH3被氧化为NO和H2O直接通入烧瓶和O2生成HNO3形成白雾,HNO3与过量的NH3反应生成NH4NO3形成白烟,化学方程式为:4NO+3O2+2H2O=4HNO3、NH3+HNO3=NH4NO3。
(2)烧杯原溶液中m(NaOH)=0.200L×1.000 mol/L×40g/mol=8g
验后将烧杯中溶液蒸干,再将所得固体加热至恒重,得到固体10.9g,溶质质量增加10.9g-8g=2.9g。
设固体中NaOH的质量为 m1(NaOH)
由关系式: NaOH-----NaNO2 质量增加
40 69 29
m1(NaOH) 2.9g
解得m1(NaOH)=4g
考点:了解常见氮元素单质及其重要化合物的主要性质及应用。掌握常见气体的实验室制法(包括所用试剂、仪器,反应原理和收集方法)。能利用化学反应方程式进行简单的化学计算。


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源:2014-2015北京市朝阳区高一上学期期末考试化学试卷(解析版) 题型:实验题
下图为铜丝与浓硫酸反应并验证其产物性质的实验装置。


(1)①中反应的化学方程式是 。其中铜发生了 (填“氧化”或“还原”)反应,判断依据为 。
(2)②中饱和NaHSO3溶液的作用是除去①中挥发出的硫酸。加热一段时间后,③中溶液依然澄清,④中溶液褪色。想要立即终止铜与硫酸的反应,最恰当的方法是 。
a.上移铜丝,使其脱离硫酸
b.撤去酒精灯
c.拔去橡胶塞倒出硫酸
(3)反应停止后,待装置冷却,把③取下后将其中溶液分成两份做如下实验:
加入试剂 | 现象 | 反应的离子方程式 | |
第一份 | 加入NaOH溶液 | 有白色沉淀生成 | ____________ |
第二份 | 加入氯水 | 有白色沉淀生成 | ____________ |
完成上述反应的离子方程式。
(4)④中棉花团的作用是 。
(5)上述实验结束后,发现①中试管内有少量白色固体出现,冷却后将试管中的物质缓缓倒入水中,溶液呈蓝色。取少量蓝色溶液于试管中,滴加NaOH溶液至过量,出现的现象是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省高三上学期期中考试化学试卷(解析版) 题型:填空题
(1)过渡金属元素铁能形成多种配合物,如:[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)]和Fe(CO)x等。
①基态Fe3+的M层电子排布式为 。
②配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x= 。Fe(CO)x常温下呈液态,熔点为 -20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于 (填晶体类型)。
(2)O和Na形成的一种只含有离子键的离子化合物的晶胞结构如图,距一个阴离子最近的所有阳离子为顶点构成的几何体为 。已知该晶胞的密度为ρg/cm3,阿伏加德罗常数为NA,求晶胞边长a= cm。(用含ρ、NA的计算式表示)

(3)原子序数小于36的X、Y、Z、M、W五种元素,其中X是原子半径最小的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,M基态原子中s电子数等于p电子数。W的原子序数为29。回答下列问题:
①Y2X2分子中Y原子轨道的杂化类型为 ,空间构型 。
②基态W原子的核外电子排布式 。
③Y、Z、M三种元素的第一电离能由大到小的顺序为 (用元素符号表示)化合物ZX3的沸点比化合物YX4的高,其主要原因是 。
④元素Y的一种氧化物与元素Z的一种氧化物互为等电子体,元素Z的这种氧化物的分子式是 。
⑤YM、ZM混合气体污染的处理方法之一是将其在催化剂作用下转化为Z的单质。
已知::①YM(g)+ 1/2M2(g)=YM2(g) △H=-283.0kJ·mol-1
②Z2(g)+ M2(g)=2ZM(g) △H=+180.5kJ·mol-1
则上述反应的热化学方程式是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省高三上学期期中考试化学试卷(解析版) 题型:选择题
下列有关化学用语使用正确的是
A.乙烯的结构简式为:CH2CH2
B.NH4C1的电子式:
C.Cr原子 的基态简化电子排布式为[Ar]3d54s1
D.S原子的外围电子排布图为
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市静安区高三上学期期末教学质量检测化学试卷(解析版) 题型:选择题
与水一样,甲醇也能微弱电离:2CH3OH(l) CH3OH2+ +CH3O-,25℃时,K=2.0×10-17。若往一定量的甲醇中加入金属钠,则有关叙述正确的是
CH3OH2+ +CH3O-,25℃时,K=2.0×10-17。若往一定量的甲醇中加入金属钠,则有关叙述正确的是
A.金属钠与甲醇反应比金属钠与水反应更剧烈
B.结合H+的能力CH3O->OH-
C.所得到溶液中K=c(CH3O-)×c(CH3OH2+)
D.所得到溶液中c(Na+)= c(CH3OH2+)+c(CH3O-)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市静安区高三上学期期末教学质量检测化学试卷(解析版) 题型:选择题
已知氧化性:Cl2> Fe3+ >I2。向FeI2溶液中加入一定量的氯水,有关离子方程式错误的是
A.2 I-+ Cl2 →I2 + 2Cl-
B.2Fe2+ + 2I-+ 2Cl2 → 2Fe3+ + I2 + 4Cl-
C.2Fe2+ + 4I-+ 3Cl2 → 2Fe3+ + 2I2 + 6Cl-
D.2Fe2+ + 6I-+ 4Cl2 → 2Fe3+ + 3I2 + 8Cl-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省益阳市高三上学期期中考试化学试卷(解析版) 题型:填空题
(9分) 向浓度相等、体积均为50 mL的A、B两份KOH溶液中,分别通入一定量的SO2气体后,再稀释到100 mL。
(1)在KOH溶液中通入一定量的SO2气体后,溶液中溶质的组成可能是:
① ;② ;
③ ;④ 。
(2)在稀释后的溶液中逐滴加入0.1 mol/L的盐酸,产生SO2的体积(标准状况)与所加盐酸的体积关系如下图所示。

①A曲线表明,原溶液通入SO2气体后,所得溶质与盐酸反应产生SO2的最大体积是____mL(标准状况)。
②B曲线表明,原溶液通入SO2气体后,所得溶液中溶质的化学式为_________________。
③原KOH溶液的物质的量浓度为________ ____。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高三1月练习理综化学试卷(解析版) 题型:填空题
某些有机化合物之间具有如下转化关系:

其中A是一种五元环状化合物,其分子中只有一种化学环境的氢原子;F核磁共振氢谱显示有三种化学环境的氢原子,且峰面积之比为2:2:3。
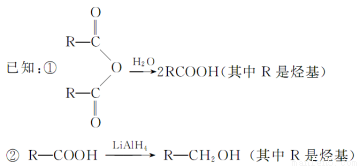
(1)G是合成顺丁橡胶的主要原料,G的名称是 。B中含氧官能团的名称是
(2)A的结构简式是
(3)⑥的化学方程式是
(4)E在一定条件下能够发生缩聚反应,其中主链上含“—CH2—”的高聚物的结构简式是 。有机物Y与E互为同分异构体,且具有相同的官能团种类和数目,则Y的结构可有 种。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com