
【题目】近年我国汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物。回答下列问题:
(l)汽车发动机工作时会引起反应:N2(g)+O2(g)![]() 2NO(g),是导致汽车尾气中含有NO的原因之一。2000K时,向容积为2L的密闭容器中充入2molN2与2molO2,发生上述反应,经过5min达到平衡,此时容器内NO的体积分数为0.75% .则该反应在5min内的平均反应速率v(O2)=_______mol/(Lmin),N2的平衡转化率为_______,2000K时该反应的平衡常数K=_____。
2NO(g),是导致汽车尾气中含有NO的原因之一。2000K时,向容积为2L的密闭容器中充入2molN2与2molO2,发生上述反应,经过5min达到平衡,此时容器内NO的体积分数为0.75% .则该反应在5min内的平均反应速率v(O2)=_______mol/(Lmin),N2的平衡转化率为_______,2000K时该反应的平衡常数K=_____。
(2)一定量NO发生分解的过程中,NO的转化率随时间变化的关系如右图所示。

① 反应2NO(g)![]() N2(g)+O2(g)为______反应(填“吸热”或“放热”) ;
N2(g)+O2(g)为______反应(填“吸热”或“放热”) ;
②一定温度下,能够说明反应2NO(g)![]() N2(g)+O2(g)已达到平衡的是_____(填序号);
N2(g)+O2(g)已达到平衡的是_____(填序号);
a.容器内的压强不发生变化
b.混合气体的密度不发生变化
c. 2NO、N2、O2的浓度保持不变
d.单位时间内分解4molNO,同时生成2molN2
③ 在四个容积和温度均完全相同的密闭容器中分别加入下列物质,相应物质的量(mol)如下表所示。相同条件下达到平衡后,N2的体积分数最大的是_______(填容器代号);
容器代号 | NO | N2 | O2 |
A | 2 | 0 | 0 |
B | 0 | l | l |
C | 0.4 | 0.6 | 0.8 |
D | l | 0.5 | 0.4 |
(3)当发动机采用稀薄燃烧时,尾气中的主要污染物为NOx。可用CH4催化还原NOx以消除氮氧化物污染。
已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574kJ·mol-1
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867kJ·mol-1
①写出CH4与NO反应生成N2、CO2、H2O(g)的热化学方程式:___________;
②使用催化剂可以将汽车尾气的主要有害成分一氧化碳(CO)和氮氧化物(NOx)转化为无毒气体,该反应的化学方程式为___________________。
【答案】 0.0015 0.75% 2.28×10-4 放热 c D CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ/mol 2xCO+2NOx![]() 2xCO2+N2
2xCO2+N2
【解析】 (1).这个反应为等体反应 ,容积为2L 将所有物质的浓度表示为N2 1mol·L-1 其余类推
N2(g)+O2(g)=2NO(g)
起 1 1 0
转 x x 2x
平 1-x 1-x 2x
![]() ,x=0.0075mol·L-1 ,v(O2)=0.0075mol/L/5min=0.0015mol/(Lmin);N2的平衡转化率为0.0075/1=0.0075;2000K时该反应的平衡常数K=
,x=0.0075mol·L-1 ,v(O2)=0.0075mol/L/5min=0.0015mol/(Lmin);N2的平衡转化率为0.0075/1=0.0075;2000K时该反应的平衡常数K=![]()
(2)①图中T2>T1,升高温度NO的转化率降低,平衡逆向移动,正向放热反应;
②a.这个反应为等体反应 ,容器内的压强保持不变化,不能说明已经达到平衡,故a错误;b.这个反应的反应物和生成物均为气体,混合气体的密度始终不发生变化,故b错误;c. 2NO、N2、O2的浓度保持不变,说明已达到平衡,C正确;d.单位时间内分解4molNO是逆速率,同时生成2molN2也是逆速率,故d错误。故选c。
③将NO转换成N2、O2后,N2、O2的量分别为
容器代号 | NO | N2 | O2 |
A | 0 | 1 | 1 |
B | 0 | l | l |
C | 0 | 0.8 | 1 |
D | 0 | 1.5 | 1.4 |
平衡后,A和BN2的体积分数相同,C中N2的体积分数最小,D中N2的体积分数最大,故选D。
(3)①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574kJ·mol-1 I
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867kJ·mol-1 Ⅱ
将Ⅱ×2-I得CH4与NO反应生成N2、CO2、H2O(g)的热化学方程式CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol-1
②使用催化剂可以将汽车尾气的主要有害成分一氧化碳(CO)和氮氧化物(NOx)转化为无毒气体,该反应的化学方程式为2xCO+2NOx![]() 2xCO2+N2
2xCO2+N2


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案科目:高中化学 来源: 题型:
【题目】在一密闭容器中进行反应2SO2 + O2![]() 2SO3,已知反应过程中某一时刻SO2、 O2、SO3的浓度分别为2 mol·L-1 、1mol·L-1 、2mol·L-1。当反应达到平衡时,容器内各物质的浓度可能为
2SO3,已知反应过程中某一时刻SO2、 O2、SO3的浓度分别为2 mol·L-1 、1mol·L-1 、2mol·L-1。当反应达到平衡时,容器内各物质的浓度可能为
A. SO2为4 mol·L-1、 O2为2 mol·L-1 B. SO3为4 mol·L-1
C. SO2为2.5 mol·L-1 D. SO2 、SO3为1.5 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用序号填写下列空格:
(1)下列各组物质
①O2和O3 ②H2、D2和T2 ③12C和14 C ④石墨和足球烯(C60)
⑤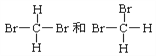 ⑥
⑥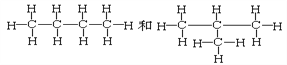
⑦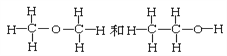 ⑧CH3CH3和CH3CH2CH2CH3
⑧CH3CH3和CH3CH2CH2CH3
互为同素异形体的是_____________;互为同位素的是______________,互为同分异构体的是______________,互为同系物的是_______________,同一种物质的是______________。
(2)现有① 金刚石 ② 干冰 ③ Na2SO4 ④ NH4Cl 四种物质,按下列要求回答:
晶体熔化时需要破坏共价键的是____________;熔点最低的是__________________;
晶体中只存在一种微粒间作用力是______________;属于离子晶体的是_____________。
请写出④ NH4Cl的电子式___________________
试判断 ①金刚石②干冰 ③Na2SO4晶体的熔点由高到低排列的顺序_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:
CO(g)+H2S(g)![]() COS(g)+H2(g) K=0.1
COS(g)+H2(g) K=0.1
反应前CO物质的量为10mol,平衡后CO物质的量为8mol。下列说法正确的是
A.升高温度,H2S浓度增加,表明该反应是吸热反应
B.通入CO后,正反应速率逐渐增大
C.反应前H2S物质的量为7mol
D.CO的平衡转化率为80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15.2MPa条件下又重复吸氢。NaAlH4可由AlCl3和NaH在适当条件下合成。NaAlH4的晶胞结构如右下图所示。

(1)基态Ti原子的价电子轨道表示式为 。
(2)NaH的熔点为800℃,不溶于有机溶剂。NaH属于 晶体,其电子式为 。
(3)AlCl3在178℃时升华,其蒸气的相对分子质量约为267,蒸气分子的结构式为 (标明配位键)。
(4)AlH4-中,Al的轨道杂化方式为 ;例举与AlH4-空间构型相同的两种离子 (填化学式)。
(5)NaAlH4晶体中,与Na+紧邻且等距的AlH4-有 个;NaAlH4晶体的密度为 g·cm-3(用含a的代数式表示)。若NaAlH4晶胞底心处的Na+被Li+取代,得到的晶体为 (填化学式)。
(6)NaAlH4的释氢机理为:每3个AlH4-中,有2个分别释放出3个H原子和1个Al原子,同时与该Al原子最近邻的Na原子转移到被释放的Al原子留下的空位,形成新的结构。这种结构变化由表面层扩展到整个晶体,从而释放出氢气。该释氢过程可用化学方程式表示为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的分类正确的是( )
A.氯化钡、四氯化碳、硫酸、碘酒都属于化合物
B.硝酸、纯碱、磷酸钠、二氧化碳分别属于酸、碱、盐、氧化物
C.溶液、浊液、胶体、空气都属于混合物
D.CO2、SO2、P2O5、CO都属于酸性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烯烃在化工生产过程中有重要意义。下面是以烯烃A为原料合成粘合剂M的路线图。

回答下列问题:
(1)下列关于路线图中的有机物或转化关系的说法正确的是_______(填字母)。
A.A能发生加成、氧化、缩聚等反应
B.B的结构简式为CH2ClCHClCH3
C.C的分子式为C4H5O3
D.M的单体是CH2=CHCOOCH3和CH2=CHCONH2
(2)A中所含官能团的名称是_______,反应①的反应类型为_________。
(3)设计步骤③⑤的目的是_________, C的名称为________。
(4)C和D生成粘合剂M的化学方程式为____________。
(5)满足下列条件的C的同分异构体共有__种(不含立体异构),写出其中核磁共振氢谱有3组峰的同分异构体的结构简式:_____________。
①能发生银镜反应 ② 酸、碱性条件下都能水解 ③ 不含环状结构
(6)结合信息,以CH3CH=CHCH2OH为原料(无机试剂任选),设计制备CH3CH=CHCOOH的合成路线。合成路线流程图示例如下:_____________
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最新研究发现,用隔膜电解法处理高浓度乙醛废水具有工艺流程简单、电耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸,
总反应为:2CH3CHO+H2O![]() CH3CH2OH+CH3COOH
CH3CH2OH+CH3COOH
实验室中,以一定浓度的乙醛—Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置示意图如图所示。

(1)若以甲烷燃料电池为直流电源,则燃料电池中b极应通入 (填化学式)气体。
(2)电解过程中,两极除分别生成乙酸和乙醇外,均产生无色气体。电极反应如下:
阳极:① 4OH--4e-=O2↑+2H2O② 。
阴极:① 。②CH3CHO+2e-+2H2O=CH3CH2OH+2OH-
(3)电解过程中,阴极区Na2SO4的物质的量 (填“增大”、“减小”或“不变”)。
(4)电解过程中,某时刻测定了阳极区溶液中各组分的物质的量,其中Na2SO4与CH3COOH的物质的量相同。下列关于阳极区溶液中各微粒浓度关系的说法正确的是 (填字母序号)。
a.c(Na+)不一定是c(SO42-)的2倍
b.c(Na+)=2c(CH3COOH)+2c(CH3COO-)
c.c(Na+)+c(H+)=c(SO42-)+c(CH3COO-)+c(OH-)
d.c(Na+)>c(CH3COOH)>c(CH3COO-)>c(OH-)
(5)高纯度氧化铝是用于制备隔膜的材料,某研究小组用以下流程制取高纯度氧化铝:

①“除杂”操作是加入过氧化氢后,用氨水调节溶液的pH约为8.0,以除去硫酸铵溶液中的少量Fe2+。请写出在除去Fe2+离子的过程中,发生的主要反应的离子方程式 。
②配制硫酸铝溶液时,需用硫酸酸化,酸化的目的是 。
③“结晶”这步操作中,母液经蒸发浓缩至溶液表面刚出现薄层晶体即停止加热,然后冷却结晶,得到铵明矾晶体(含结晶水)。母液不能蒸干的原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含有CaCO3固体的溶液中滴加少许浓盐酸(忽略体积变化),下列数值变小的是( )
A.c(H+) B. c(Ca2+) C. c(CO32-) D. Ksp(CaCO3)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com