
| A. | 同浓度的AOH溶液和H2B溶液,电离程度前者大于后者 | |
| B. | HB-的电离程度大于HB-的水解程度 | |
| C. | 该盐的电离方程式为AHB═A++H++B2- | |
| D. | 在溶液中离子浓度大小顺序一般为.c(A+)>c(HB-)>c(OH-)>c(B2-)>c(H+) |
分析 酸式盐AHB,它的水溶液呈弱碱性,说明该盐中阴离子的水解程度大于电离程度,或是一种强碱弱酸盐,根据水解原理以及电离情况来判断.
解答 解:酸式盐AHB,它的水溶液呈弱碱性,说明该盐中阴离子的水解程度大于电离程度,或是一种强碱弱酸盐,
A.若是强碱弱酸盐,则相同物质的量浓度的AOH溶液和H2B溶液,前者的电离程度大于后者的电离程度,故A正确;
B.酸式盐AHB,它的水溶液呈弱碱性,说明该盐中阴离子的水解程度大于电离程度,HB-的电离程度小于HB-的水解程度,故B错误;
C.该盐溶液的电离方程式一般写成:AHB=A++HB-,HB-?H++B2-,故C错误;
D.酸式盐AHB,它的水溶液呈弱碱性,说明该盐中阴离子的水解程度大于电离程度,溶液中离子浓度大小为:c(A+)>c(HB-)>c(B2-)>c(OH-)>c(H+),故D错误,
故选A.
点评 本题考查学生盐的水解原理以及电解质的电离知识,注意电离和水解程度大小的比较,注意知识的归纳和梳理是解题的关键,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤⑥ | B. | ②③④⑤⑥ | C. | ②⑤⑥ | D. | ①②⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | 只有⑤ | C. | ③④⑤ | D. | 只有①②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②①③ | B. | ③②① | C. | ②③① | D. | ①③② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑤ | B. | ①⑤ | C. | ①②③⑧ | D. | ④⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
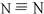 ,氮的氢化物除了氨气,还有一种在常温下呈液态的肼,分子式为N2H4,请写出肼的电子式
,氮的氢化物除了氨气,还有一种在常温下呈液态的肼,分子式为N2H4,请写出肼的电子式 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 密闭容器中2molNO与1molO2充分反应后,容器内气体的分子数为2NA | |
| B. | 用惰性电极电解CuSO4溶液后,如果加入0.1molCu(OH)2能使溶液复原,则电路中转移电子的数目为0.2NA | |
| C. | 标准状况下,2.24LCl2溶于足量NaOH中转移电子的数目为0.1NA | |
| D. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com