
下列离子方程式中,正确的是( )
A.铜粉加入到Fe2(SO4)3溶液中:3Cu+2Fe3+===2Cu2++2Fe
B.钠块投入到CuSO4溶液中:2Na+Cu2+===2Na++Cu↓
C.Cl2通入到NaOH溶液中:Cl2+2OH-===Cl-+ClO-+H2O
D.用NaOH溶液吸收少量CO2:OH-+CO2===HCO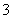
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
.S(单斜)和S(正交)是硫的两种同素异形体。
已知:①S(单斜,s)+O2(g)===SO2(g)
ΔH1=-297.16 kJ·mol-1
②S(正交,s)+O2(g)===SO2(g)
ΔH2=-296.83 kJ·mol-1
③S(单斜,s)===S(正交,s) ΔH3
下列说法正确的是( )
A.ΔH3=0.33 kJ·mol-1
B.单斜硫转化为正交硫的反应是吸热反应
C.S(单斜,s)===S(正交,s) ΔH3<0,正交硫比单斜硫稳定
D.S(单斜,s)===S(正交,s) ΔH3>0,单斜硫比正交硫稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应条件的控制中不恰当的是
( )。
A.为防止铁生锈,在其表面涂一层防锈油漆
B.为防止火灾,在面粉厂、加油站等场所要严禁烟火
C.为加快KClO3的分解速率,加入MnO2
D.为加快H2O2的分解速率,把反应容器放到冷水中冷却
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计。
锌片上发生的电极反应______________________________________
银片上发生的电极反应______________________________________
(2)若该电池中两电极的总质量为60 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47 g,试计算:
①产生氢气的体积(标准状况);②通过导线的电量。(已知NA=6.02×1023 mol-1,电子电荷为1.60×10-19 C)
查看答案和解析>>
科目:高中化学 来源: 题型:
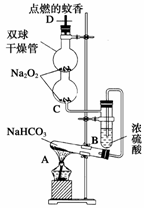
如图是研究二氧化硫性质的微型实验装置。现用60%硫酸溶液和亚硫酸钠晶体反应制取SO2气体,实验现象很明显,且不易污染空气。下列说法中错误的是( )
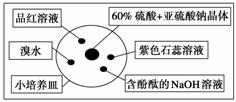
A.紫色石蕊溶液变蓝色 B.品红溶液褪色
C.溴水橙色褪去 D.含酚酞的NaOH溶液红色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
请分析回答某同学在探究浓硫酸、稀硫酸、浓硝酸、稀硝酸分别与铜反应的实验中发生的有关问题。
Ⅰ.探究上述四种酸的氧化性相对强弱及其与铜反应的还原产物的性质:
(1)分别向盛有等量铜片的四支试管中加入等体积的①浓硫酸 ②稀硫酸 ③浓硝酸 ④稀硝酸,能随即发生反应的是(填序号,下同)____________,微热则发生反应的是____________,加热后发生反应的是__________,加热也不发生反应的是____________。由此可以得到上述四种酸氧化性由强到弱的顺序是__________________________________。
(2)
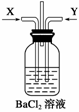
先将铜与浓硫酸反应产生的气体X持续通入如右图所示装置中,一段时间后再将铜与浓硝酸反应产生的大量气体Y也持续通入该装置中,可观察到的现象包括________(选填序号)。
A.通入X气体后产生白色沉淀 B.通入X气体后溶液中无明显现象
C.通入Y气体开始产生沉淀 D.通入Y气体后沉淀溶解
E.通入Y气体后溶液中无明显现象
(3)由此可得到的结论是________(选填序号)。
A.HNO3的酸性比H2SO4强 B.盐酸的酸性比H2SO3强
C.BaSO3能溶于盐酸 D.HNO3能氧化H2SO3(或SO2)
E.BaSO4不溶于水也不溶于HNO3溶液
Ⅱ.下图是甲、乙两位同学探究铜与稀硝酸反应还原产物的实验装置图,请回答下列问题:
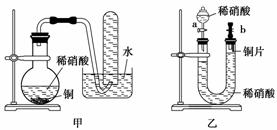
(1)写出铜和稀硝酸反应的离子方程式:_____________________________________。
(2)实验装置甲能否证明铜和稀硝酸反应的产物是NO气体________(填“能”或“不能”),请简述理由(用文字和化学方程式表示):__________________________________
________________________________________________________________________。
(3)若用实验装置乙进行实验,检查装置气密性的操作是_______________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
联合国卫生组织认为我国的铁锅是一种理想的炊具而向世界推广。其主要原因是( )
A.升热慢,退热也慢,保温性能好
B.烹饪的食物中含丰富的“铁质”
C.生产过程简单,价格便宜
D.生铁中含碳元素,因而含有对人体有益的有机物
查看答案和解析>>
科目:高中化学 来源: 题型:
根据图中反应,写出各物质的化学式及①②③反应的化学方程式。
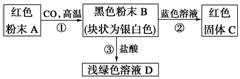
(1)A是________,B是________,C是________,D是________。
(2)化学方程式:
①________________________________________________________________________;
②________________________________________________________________________;
③________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com