
| A. | 6ml | B. | 12ml | C. | 15ml | D. | 18ml |
分析 常温常压下,将24ml的氧气和硫化氢的混合气体点火燃烧,充分冷却反应后到原来状态,测得有6mL二氧化硫生成,根据反应2H2S+3O2═2SO2+2H2O可知,生成6mL二氧化硫消耗硫化氢和氧气的总体积为:6mL×$\frac{2+3}{2}$=15mL;剩余的气体发生反应2H2S+O2═2S↓+2H2O,结合反应方程式计算出混合气体中硫化氢的总体积.
解答 解:有二氧化硫生成,说明发生了反应2H2S+3O2═2SO2+2H2O,根据反应可知生成6mL二氧化硫消耗硫化氢和氧气的总体积为:6mL×$\frac{2+3}{2}$=15mL,其含有硫化氢的体积为:15mL×$\frac{2}{5}$=6mL;
剩余气体体积为:24mL-15mL=9mL,剩余发生反应2H2S+O2═2S↓+2H2O,则反应生成S单质的硫化氢的体积为:9mL×$\frac{2}{3}$=6mL,
所以原混合气体中硫化氢的总体积为:6mL+6mL=12mL,
故选B.
点评 本题考查了化学方程式的计算,题目难度中等,明确发生反应实质为解答关键,注意硫化氢与氧气的反应中,氧气不足时生成S,氧气过量时生成二氧化硫,试题侧重考查学生的分析、理解能力及化学计算能力.


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:推断题
 X、Y、Z、U、W是原子序数依次增大的前四周期元素.其中Y的原子核外有7种运动状态不同的电子;X、Z中未成对电子数均为2; U是第三周期元素形成的简单离子中半径最小的元素;W的内层电子全充满,最外层只有1个电子.请回答下列问题:
X、Y、Z、U、W是原子序数依次增大的前四周期元素.其中Y的原子核外有7种运动状态不同的电子;X、Z中未成对电子数均为2; U是第三周期元素形成的简单离子中半径最小的元素;W的内层电子全充满,最外层只有1个电子.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16.9 g BaO2固体中阴、阳离子总数为0.2NA | |
| B. | 标况下,5.6 L NO和5.6 L O2的混合气体中含有的分子数为0.375NA | |
| C. | 标准状况下,11.2 L乙烯含有的极性共价键数目为NA | |
| D. | 100 mL 0.1 mol•L-1的硫酸铝溶液中含有的Al3+为0.02NA个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如下.该电池工作时,下列说法正确的是( )
Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如下.该电池工作时,下列说法正确的是( )| A. | Mg电极是该电池的正极 | |
| B. | H2O2在石墨电极上发生氧化反应 | |
| C. | 石墨电极附近溶液的OH-的物质的量浓度增大 | |
| D. | 溶液中Cl-向正极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,浓硫酸可以用铁制槽罐存放,说明铁与浓硫酸不反应 | |
| B. | 检验氯化氢中是否混有氯气,可采用湿润的有色布条 | |
| C. | 镁在空气中燃烧只生成氧化镁 | |
| D. | 钠可以从硫酸铜溶液中置换出金属铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | H | Li | Be | B | C | N | O | F |
| 电负性 | 2.1 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 |
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.7 | 2.1 | 2.3 | 3.0 | 0.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
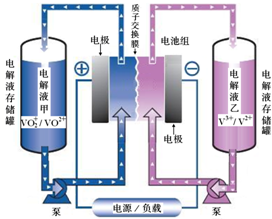 (1)全钒液流电池储能技术及应用荣获2015年国家技术发明二等奖.其结构及工作原理如图所示,电解液均呈酸性.
(1)全钒液流电池储能技术及应用荣获2015年国家技术发明二等奖.其结构及工作原理如图所示,电解液均呈酸性.| 化学式 | 电离常数 |
| HCN | K=6.2×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.4×10-7 K2=4.7×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
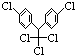 ,有关它的说法正确的是( )
,有关它的说法正确的是( )| A. | 它属于芳香烃 | B. | 分子中最多有23个原子共面 | ||
| C. | 分子式为C14H8Cl5 | D. | 1 mol该物质能与6 molH2加成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com